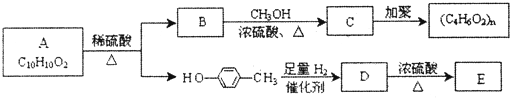
题目内容
美国化学家R.F.Heck因发现如下Heck反应而获得2010年诺贝尔化学奖.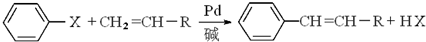 (X为卤原子,R为取代基)
(X为卤原子,R为取代基)
经由Heck反应合成M(一种防晒剂)的路线如下: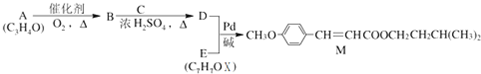
回答下列问题:
(1)A物质中含有的官能团名称是 .
(2)M可发生的反应类型是 .
a.取代反应 b.酯化反应 c.缩聚反应 d.加成反应
(3)写出结构简式:B ,E ,D .
(4)在A→B的反应中,检验A是否反应完全的试剂是 .
(5)C与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,F的结构简式是 .
(6)E的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上的一取代物只有两种同分异构体,K与FeCl3溶液作用显紫色.K与过量NaOH溶液共热,发生反应的方程式为 .
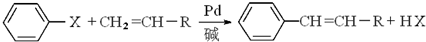 (X为卤原子,R为取代基)
(X为卤原子,R为取代基)经由Heck反应合成M(一种防晒剂)的路线如下:

回答下列问题:
(1)A物质中含有的官能团名称是
(2)M可发生的反应类型是
a.取代反应 b.酯化反应 c.缩聚反应 d.加成反应
(3)写出结构简式:B
(4)在A→B的反应中,检验A是否反应完全的试剂是
(5)C与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,F的结构简式是
(6)E的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上的一取代物只有两种同分异构体,K与FeCl3溶液作用显紫色.K与过量NaOH溶液共热,发生反应的方程式为
考点:有机物的推断
专题:有机物的化学性质及推断
分析:由合成M的结构、E的分子式(C7H8O)及反应信息,可知E应为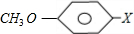 ,D为CH2═CHCOOCH2CH2CH(CH3)2,A发生氧化反应生成B,B与C反应生成D,结合A的分子式与D的结构,可推知B为CH2═CH-COOH,C为HOCH2CH2CH(CH3)2,则A为CH2═CH-CHO,据此解答.
,D为CH2═CHCOOCH2CH2CH(CH3)2,A发生氧化反应生成B,B与C反应生成D,结合A的分子式与D的结构,可推知B为CH2═CH-COOH,C为HOCH2CH2CH(CH3)2,则A为CH2═CH-CHO,据此解答.
 ,D为CH2═CHCOOCH2CH2CH(CH3)2,A发生氧化反应生成B,B与C反应生成D,结合A的分子式与D的结构,可推知B为CH2═CH-COOH,C为HOCH2CH2CH(CH3)2,则A为CH2═CH-CHO,据此解答.
,D为CH2═CHCOOCH2CH2CH(CH3)2,A发生氧化反应生成B,B与C反应生成D,结合A的分子式与D的结构,可推知B为CH2═CH-COOH,C为HOCH2CH2CH(CH3)2,则A为CH2═CH-CHO,据此解答.解答:
解:由合成M的结构、E的分子式(C7H8O)及反应信息,可知E应为 ,D为CH2═CHCOOCH2CH2CH(CH3)2,A发生氧化反应生成B,B与C反应生成D,结合A的分子式与D的结构,可推知B为CH2═CH-COOH,C为HOCH2CH2CH(CH3)2,则A为CH2═CH-CHO,
,D为CH2═CHCOOCH2CH2CH(CH3)2,A发生氧化反应生成B,B与C反应生成D,结合A的分子式与D的结构,可推知B为CH2═CH-COOH,C为HOCH2CH2CH(CH3)2,则A为CH2═CH-CHO,
(1)由上述分析可知,A为CH2═CH-CHO,含有官能团有:碳碳双键、醛基,故答案为:碳碳双键、醛基;
(2)M分子中含有碳碳双键、苯环,可以发生加成反应;含有苯环、酯基等可以发生取代反应,不能发生酯化反应与缩聚反应,故选:ad;
(3)由上述分析可知,B为CH2═CH-COOH,E为 ,D为CH2═CHCOOCH2CH2CH(CH3)2,
,D为CH2═CHCOOCH2CH2CH(CH3)2,
故答案为:CH2═CH-COOH; ;CH2═CHCOOCH2CH2CH(CH3)2;
;CH2═CHCOOCH2CH2CH(CH3)2;
(4)在A→B的反应中,醛基转化为羧基,用新制Cu(OH)2悬浊液(或新制银氨溶液)检验A是否否反应完全,故答案为:新制Cu(OH)2悬浊液(或新制银氨溶液);
(5)C为HOCH2CH2CH(CH3)2,与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,故C发生消去反应生成F,所以F为(CH3)2CHCH=CH2,故答案为:(CH3)2CHCH=CH2;
(6)E的一种同分异构体K苯环上有两个取代基且苯环上只有两种不同化学环境的氢,说明两个取代基处于苯环的对位位置,K与FeCl3溶液作用显紫色,则K中含有酚羟基.故K为 ,K与过量NaOH溶液共热,酚羟基与碱发生中和反应,-X原子在氢氧化钠水溶液、加热条件发生取代反应,发生反应的方程式为
,K与过量NaOH溶液共热,酚羟基与碱发生中和反应,-X原子在氢氧化钠水溶液、加热条件发生取代反应,发生反应的方程式为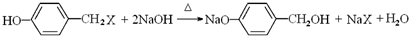 ,
,
故答案为: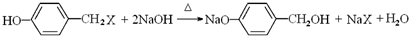 .
.
 ,D为CH2═CHCOOCH2CH2CH(CH3)2,A发生氧化反应生成B,B与C反应生成D,结合A的分子式与D的结构,可推知B为CH2═CH-COOH,C为HOCH2CH2CH(CH3)2,则A为CH2═CH-CHO,
,D为CH2═CHCOOCH2CH2CH(CH3)2,A发生氧化反应生成B,B与C反应生成D,结合A的分子式与D的结构,可推知B为CH2═CH-COOH,C为HOCH2CH2CH(CH3)2,则A为CH2═CH-CHO,(1)由上述分析可知,A为CH2═CH-CHO,含有官能团有:碳碳双键、醛基,故答案为:碳碳双键、醛基;
(2)M分子中含有碳碳双键、苯环,可以发生加成反应;含有苯环、酯基等可以发生取代反应,不能发生酯化反应与缩聚反应,故选:ad;
(3)由上述分析可知,B为CH2═CH-COOH,E为
 ,D为CH2═CHCOOCH2CH2CH(CH3)2,
,D为CH2═CHCOOCH2CH2CH(CH3)2,故答案为:CH2═CH-COOH;
 ;CH2═CHCOOCH2CH2CH(CH3)2;
;CH2═CHCOOCH2CH2CH(CH3)2;(4)在A→B的反应中,醛基转化为羧基,用新制Cu(OH)2悬浊液(或新制银氨溶液)检验A是否否反应完全,故答案为:新制Cu(OH)2悬浊液(或新制银氨溶液);
(5)C为HOCH2CH2CH(CH3)2,与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,故C发生消去反应生成F,所以F为(CH3)2CHCH=CH2,故答案为:(CH3)2CHCH=CH2;
(6)E的一种同分异构体K苯环上有两个取代基且苯环上只有两种不同化学环境的氢,说明两个取代基处于苯环的对位位置,K与FeCl3溶液作用显紫色,则K中含有酚羟基.故K为
 ,K与过量NaOH溶液共热,酚羟基与碱发生中和反应,-X原子在氢氧化钠水溶液、加热条件发生取代反应,发生反应的方程式为
,K与过量NaOH溶液共热,酚羟基与碱发生中和反应,-X原子在氢氧化钠水溶液、加热条件发生取代反应,发生反应的方程式为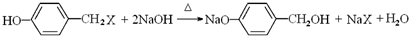 ,
,故答案为:
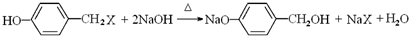 .
.
点评:本题考查有机信息合成与推断、同分异构体、官能团的结构与性质等,需要学生对给予的信息进行利用,较好的考查学生自学能力与知识迁移应用,理解题目信息是解题的关键,难度中等.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
目前人类已发现几千万种物质,对物质进行分类,有利于我们的学习,下列物质的分类不正确的是( )
| A、SO2(氧化物) |
| B、稀硫酸(电解质) |
| C、HNO3(含氧酸) |
| D、氯水(混合物) |
能说明NH4+的5个原子不在同一平面而为正四面体结构的是( )
| A、键长相同,两个键之间夹角为109°28′ |
| B、N-H键为极性共价键 |
| C、4个N-H键的键能、键长相同 |
| D、N-H原子间存在配位键 |
下列叙述中,正确的是( )
| A、在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低 |
| B、常温下,pH=4的溶液一定是酸溶液 |
| C、FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
| D、在滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,说明BaCl2溶液有酸性 |
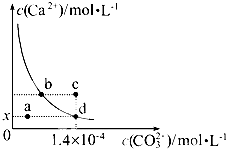 室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9,下列说法不正确的是( )
室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9,下列说法不正确的是( )| A、加入蒸馏水可使溶液由d点变到a点 |
| B、c点时有碳酸钙沉淀生成 |
| C、x数值为2×10-5 |
| D、b点与d点对应的溶度积相等 |
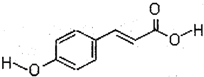 [化学一选修/有机化学基础]
[化学一选修/有机化学基础]