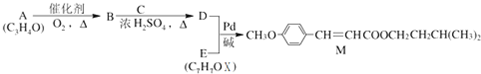
题目内容
能说明NH4+的5个原子不在同一平面而为正四面体结构的是( )
| A、键长相同,两个键之间夹角为109°28′ |
| B、N-H键为极性共价键 |
| C、4个N-H键的键能、键长相同 |
| D、N-H原子间存在配位键 |
考点:判断简单分子或离子的构型,键能、键长、键角及其应用
专题:化学键与晶体结构
分析:键角是描述分子立体结构的重要参数,键长和键能是衡量共价键稳定性的主要参数,据此分析.
解答:
解:A、键长是衡量共价键稳定性的主要参数,键长相同,两个键之间夹角为109°28′能说明该微粒的空间结构为正四面体,故A正确;
B、N-H键为极性共价键,与分子的空间构型无关,故B错误;
C、键能是衡量共价键稳定性的主要参数,NH4+的N-H键能相同,不能判断分子的空间构型,故C错误;
D、N-H原子间存在配位键,不说明分子的空间构型为正四面体,故D错误;
故选A.
B、N-H键为极性共价键,与分子的空间构型无关,故B错误;
C、键能是衡量共价键稳定性的主要参数,NH4+的N-H键能相同,不能判断分子的空间构型,故C错误;
D、N-H原子间存在配位键,不说明分子的空间构型为正四面体,故D错误;
故选A.
点评:本题考查了微粒的空间结构,题目难度不大,注意把握共价键的键参数对分子性质的影响.

练习册系列答案
相关题目
下列设备工作时,将化学能转化为热能的是( )
A、 硅太阳能电池 |
B、 锂离子电池 |
C、 太阳能集热器 |
D、 燃气炉 |
将足量的AgCl分别加入下列物质中,AgCl的溶解度由大到小的排列顺序是( )
①20ml0.01mol∕LKCl溶液;
②20ml0.02mol∕LCaCl2溶液;
③20ml蒸馏水;
④20ml0.03mol∕LHCl溶液;
⑤20ml0.05mol∕L AgNO3溶液.
①20ml0.01mol∕LKCl溶液;
②20ml0.02mol∕LCaCl2溶液;
③20ml蒸馏水;
④20ml0.03mol∕LHCl溶液;
⑤20ml0.05mol∕L AgNO3溶液.
| A、①>②>④>③>⑤ |
| B、③>①>④>②>⑤ |
| C、⑤>③>②>①>④ |
| D、③>④>⑤>②>① |
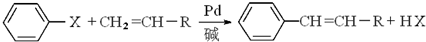 (X为卤原子,R为取代基)
(X为卤原子,R为取代基)