题目内容
19.亚氯酸钠(NaClO2)是一种高效氧化剂和优质漂白剂.一种以氯酸钠(NaClO3)为原料制备NaClO2粗品的工艺流程如图所示: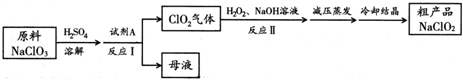
已知:
①纯ClO2易分解爆炸,空气中ClO2的体积分数在10%以下比较安全;
②NaClO2在碱性溶液中稳定存在,在酸性溶液中迅速分解;
③含水NaClO2受热易分解.
(1)试剂A可以选择a(填字母序号).
a.SO2 b.浓硝酸 c.KMnO4
(2)下列关于上述流程的说法中,合理的是ac(填字母序号).
a.反应Ⅰ进行过程中应持续鼓入空气
b.反应Ⅰ后得到的母液中,溶质的主要成分是NaCl
c.反应Ⅱ中NaOH 应过量
(3)反应Ⅱ的离子方程式为2ClO2+H2O2+2OH-═2ClO2-+2H2O+O2.
(4)已知压强越大,物质的沸点越高.反应Ⅱ结束后采用“减压蒸发”操作的原因是在较低温度蒸发浓缩,可防止温度过高NaClO2分解.
(5)NaClO2变质可分解为NaClO3和NaCl.取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量相同.(填“相同”,“不同”或“无法判断”)
(6)中间产物二氧化氯(ClO2)在生产生活中也有广泛应用.用ClO2处理泄漏的氰化钠
(NaCN),得到无毒的NaCl、N2 和CO2.若处理含NaCN 4×10-5mol•L-1的废水 1000L,至少需要ClO2 的质量为2.7g.
(7)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备.写出该制备反应的化学方程式5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O.
分析 NaClO3和浓H2SO4在反应器I中发生还原反应生成ClO2和Na2SO4,所以试剂A可以用二氧化硫,ClO2在反应器II中与双氧水、氢氧化钠反应生成亚氯酸钠,再得到其晶体,
(1)根据上面的分析可判断试剂A;
(2)根据信息纯ClO2易分解爆炸,空气中ClO2的体积分数在10%以下比较安全,所以要持续通过量的空气,NaClO2在碱性溶液中稳定存在,在酸性溶液中迅速分解,所以反应Ⅱ中碱要过量,因为试剂A为二氧化硫,NaClO3被还原成ClO2,所以反应Ⅰ后得到的母液中,溶质的主要成分是Na2SO4;
(3)反应Ⅱ中ClO2被双氧水还原成ClO2-,根据元素守恒和电荷守恒书写的离子方程式;
(4)含水NaClO2受热易分解,所以亚氯酸钠溶液中获得晶体,温度不能太高;
(5)取等质量变质前后的NaClO2试样足量FeSO4溶液反应时,最后氯元素都被还原成氯离子,NaClO2变质可分解为NaClO3和NaCl,是氯元素的自身氧化还原,根据电子得失守恒可知,整个过程中电子转移数目相同,据此判断;
(6)用ClO2处理泄漏的氰化钠(NaCN),得到无毒的NaCl、N2 和CO2,根据电子得失守恒可知关系式ClO2~NaCN,根据NaCN 的物质的量,结合关系式可计算出需要ClO2 的质量;
(7)在酸性条件下,NaClO2发生自身氧化还原得ClO2和aCl,根据元素守恒和电子得失守恒书写化学方程式.
解答 解:NaClO3和浓H2SO4在反应器I中发生还原反应生成ClO2和Na2SO4,所以试剂A可以用二氧化硫,ClO2在反应器II中与双氧水、氢氧化钠反应生成亚氯酸钠,再得到其晶体,
(1)根据上面的分析可知试剂A为SO2,故选a;
(2)根据信息纯ClO2易分解爆炸,空气中ClO2的体积分数在10%以下比较安全,所以要持续通过量的空气,NaClO2在碱性溶液中稳定存在,在酸性溶液中迅速分解,所以反应Ⅱ中碱要过量,因为试剂A为二氧化硫,NaClO3被还原成ClO2,所以反应Ⅰ后得到的母液中,溶质的主要成分是Na2SO4,
故选ac;
(3)反应Ⅱ中ClO2被双氧水还原成ClO2-,反应的离子方程式为2ClO2+H2O2+2OH-═2ClO2-+2H2O+O2,
故答案为:2ClO2+H2O2+2OH-═2ClO2-+2H2O+O2;
(4)含水NaClO2受热易分解,所以亚氯酸钠溶液中获得晶体,温度不能太高,所以反应Ⅱ结束后采用“减压蒸发”操作,在较低温度蒸发浓缩,可防止温度过高NaClO2分解,
故答案为:在较低温度蒸发浓缩,可防止温度过高NaClO2分解;
(5)取等质量变质前后的NaClO2试样足量FeSO4溶液反应时,最后氯元素都被还原成氯离子,NaClO2变质可分解为NaClO3和NaCl,是氯元素的自身氧化还原,根据电子得失守恒可知,整个过程中电子转移数目相同,所以消耗Fe2+的物质的量相同,
故答案为:相同;
(6)用ClO2处理泄漏的氰化钠(NaCN),得到无毒的NaCl、N2 和CO2,根据电子得失守恒可知关系式ClO2~NaCN,NaCN 的物质的量为 4×10-5mol•L-1×1000L=0.04mol,结合关系式可计算出需要ClO2 的质量为0.04mol×67.5g/mol=2.7g,
故答案为:2.7;
(7)在酸性条件下,NaClO2发生自身氧化还原得ClO2和aCl,该反应的化学方程式为5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O,
故答案为:5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O.
点评 本题考查物质的制备实验的工业设计,题目难度中等,本题注意把握物质的性质,从质量守恒的角度以及氧化还原反应的特点判断生成物,为解答该题的关键,也是易错点

 智慧小复习系列答案
智慧小复习系列答案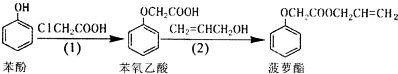
下列叙述错误的是( )
| A. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 | |
| B. | 苯酚、苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 | |
| C. | 步骤(1)中由苯酚生成苯氧乙酸的反应属于取代反应 | |
| D. | 可用溴水检验步骤(2)的产物中是否有烯丙醇(CH2=CHCH2OH) 残留 |
| A. | c(Cl-)>c(NH4+)>c(OH-)>c(H+) | B. | c(Cl-)>c(NH4+)>c(H+)>c(OH-) | ||
| C. | c(H+)>c(OH-)>c(Cl-)>c(NH4+) | D. | c(H+)>c(Cl-)>c(NH4+)>c(OH-) |
| A. | 若Q1+Q2<Q3,则反应为放热反应 | B. | 若Q1+Q2<2Q3,则反应为放热反应 | ||
| C. | 若E1+E2>E3,则反应为放热反应 | D. | 若E1+E2>E3,则反应为吸热反应 |

