题目内容
1.在含有0.078molFeCl2溶液中通入0.009molCl2,再加入含有0.01molX2O72-的酸性溶液,使溶液中的Fe2+恰好全部氧化,并使X2O72-还原成xn+离子,n值为( )| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
分析 0.078molFe2+被氧化为0.078molFe3+,失去0.078mol电子,利用电子守恒,0.009molCl2与0.01molX2O72-也应该得到0.078mol电子,令X在还原产物的化合价为a,根据电子转移守恒列放出计算a值,即为n值.
解答 解:0.078molFe2+被氧化为0.078molFe3+,失去0.078mol电子,利用电子守恒,0.009molCl2与0.01molX2O72-也应该得到0.078mol电子,令X在还原产物的化合价为a,则:
0.009mol×2+0.01mol×2×(6-a)=0.078mol
解得a=3,
则n值为3,
故选:B.
点评 本题考查氧化还原反应的计算,难度中等,注意理解电子转移守恒的运用.

练习册系列答案
相关题目
12.下列说法不正确的是( )
| A. | 铝制品经久耐用的原因是在空气中其表面可形成致密的氧化膜 | |
| B. | Na-K合金可用于原子反应堆的导热剂 | |
| C. | 漂白粉可敞口保存 | |
| D. | AgI可用于人工降雨 |
9.下列有关化学用语表示正确的是( )
| A. | N2的电子式: | |
| B. | 质子数为53、中子数为78的碘原子:${\;}_{53}^{131}$I | |
| C. | S2-的结构示意图: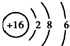 | |
| D. | O原子的基态电子排布式为:1s22s22p${\;}_{x}^{2}$p${\;}_{y}^{2}$p${\;}_{z}^{0}$. |
16.学习卤素后发现一种规律,某元素的单质或化合物通过缔合易溶于该元素的化合物中,如I2易溶于KI溶液中,HF易溶于NaF溶液中,属于上述情况的是( )
| A. | Br2易用于溴苯中 | B. | S易用于CS2中 | ||
| C. | S易溶于Na2S溶液中 | D. | AgF易溶于水中 |
6.向一定量的Fe、FeO和Fe2O3的混合物中加入100ml 2mol/L的盐酸,恰好使混合物完全溶解,放出44.8ml标准状况下的气体,所得溶液中,加入溶液无红色出现,那么若用一氧化碳在高温下还原相同质量的此混合物,能得到铁的质量( )
| A. | 5.6g | B. | 2.8 g | C. | 11.2g | D. | 无法计算 |
13.化学与生活、科学、技术、社会、环境密切相关,下列有关说法中错误的是( )
| A. | 高纯硅可作计算机芯片的材料 | |
| B. | 洁厕灵的主要成分是盐酸,不能与“84”消毒液(主要成分是NaClO)混用 | |
| C. | PM2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体 | |
| D. | Na2SiO3溶液可做木材防火剂 |
10.NA代表阿伏加德罗常数.下列有关NA的叙述中,正确的是( )
| A. | 1mol 任何物质所含的分子数均为NA | |
| B. | 14g氮气所含的氮原子数为NA | |
| C. | 44gCO2与28gCO所含的分子数均为NA | |
| D. | NA个氢气分子和NA个氯气分子的质量比为1:1 |
8.等质量的下列烃完全燃烧时,消耗氧气最多的是( )
| A. | CH4 | B. | C2H4 | C. | C2H6 | D. | C6H8 |