题目内容
13.化学与生活、科学、技术、社会、环境密切相关,下列有关说法中错误的是( )| A. | 高纯硅可作计算机芯片的材料 | |
| B. | 洁厕灵的主要成分是盐酸,不能与“84”消毒液(主要成分是NaClO)混用 | |
| C. | PM2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体 | |
| D. | Na2SiO3溶液可做木材防火剂 |
分析 A.计算机芯片芯片的成分硅单质;
B.洁厕灵(含盐酸)和84消毒液(含次氯酸钠)进行混用,会产生有毒气体氯气;
C.胶体粒子的直径介于1nm~100nm之间;
D.木材和织物用水玻璃浸泡后既可防腐又不易着火.
解答 解:A.高纯硅可以作计算机芯片材料,故A正确;
B.洁厕灵(含盐酸)和84消毒液(含次氯酸钠)进行混用,会产生有毒气体氯气,所以不能与“84“消毒液混用,故B正确;
C.胶体粒子的直径介于1nm~100nm之间,PM2.5是指大气中直径≤2.5×10-6m的颗粒物,不一定为胶体,故C错误;
D.木材和织物用水玻璃浸泡后既可防腐又不易着火,可做木材防火剂,故D正确.
故选C.
点评 本题考查化学与社会、环境的关系,把握常见物质的性质以及用途为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
1.在含有0.078molFeCl2溶液中通入0.009molCl2,再加入含有0.01molX2O72-的酸性溶液,使溶液中的Fe2+恰好全部氧化,并使X2O72-还原成xn+离子,n值为( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
8.有关盐类水解应用的叙述不正确的是( )
| A. | 热的纯碱溶液去污能力增强 | |
| B. | 配制FeCl3溶液,可加入少量的稀硫酸,以防止溶液浑浊 | |
| C. | 加热蒸干Al2(SO4)3溶液,最终能得到Al2(SO4)3晶体 | |
| D. | 利用明矾净水 |
18.“轨道”2Px与3Py上电子一定相同的方面是( )
| A. | 能量 | B. | 呈纺锤形 | ||
| C. | 自旋方向 | D. | 在空间的伸展方向 |
5.下列有关铁及其化合物的说法中正确的是( )
| A. | 赤铁矿的主要成分是Fe3O4 | |
| B. | 铁与水蒸气在高温下的反应产物为Fe2O3和H2 | |
| C. | 除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤 | |
| D. | Fe3+与KSCN产生红色沉淀,铁与水蒸气在高温下的反应产物为Fe3O4和H2 |
20.消除氮氧化物污染有多种方法.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4 (g)+4NO2 (g)═4NO(g)+CO2(g)+2H2 O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)═2N2 (g)+CO2(g)+2H2 O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(1),△H=-955 kJ•mol-1.
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
①不能作为判断反应达到化学平衡状态的依据是B C
A.容器内CO2的浓度保持不变 B.v正(N2)=2v正(NO) C.容器内压强保持不变 D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②计算该温度下该反应的平衡常数为0.56(保留两位小数);
③在30min,改变某一条件,反应重新达到平衡,则改变的条件是减小CO2浓度.
(3)甲烷燃料电池可以提升能量利用率,如图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:
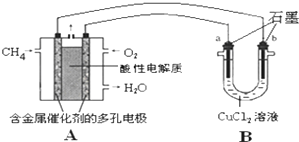
请回答:
①甲烷燃料电池的负极反应式是CH4-8e─+2H2O=CO2+8H+
②当A中消耗0.15mol氧气时,B中b(用a或b 表示)极增重19.2g.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4 (g)+4NO2 (g)═4NO(g)+CO2(g)+2H2 O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)═2N2 (g)+CO2(g)+2H2 O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(1),△H=-955 kJ•mol-1.
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
A.容器内CO2的浓度保持不变 B.v正(N2)=2v正(NO) C.容器内压强保持不变 D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②计算该温度下该反应的平衡常数为0.56(保留两位小数);
③在30min,改变某一条件,反应重新达到平衡,则改变的条件是减小CO2浓度.
(3)甲烷燃料电池可以提升能量利用率,如图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:

请回答:
①甲烷燃料电池的负极反应式是CH4-8e─+2H2O=CO2+8H+
②当A中消耗0.15mol氧气时,B中b(用a或b 表示)极增重19.2g.

 二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.
二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.