题目内容
5.下列对各组金属性质的比较中,正确的是( )| A. | 熔点:Li<Na<K | B. | 金属性:Al<Mg | C. | 密度:Na>Mg>Al | D. | 硬度:Mg<K |
分析 A、对于碱金属元素,从上而下,单质的熔点逐渐降低;
B、同一周期从左到右,元素的金属性逐渐减弱;
C、钠镁铝的密度逐渐增大;
D、通常金属越活泼,则硬度越小.
解答 解:A、对于碱金属元素,从上而下,单质的熔点逐渐降低,故熔点Li>Na>K,故A错误;
B、同一周期从左到右,元素的金属性逐渐减弱,故金属性Al<Mg,故B正确;
C、钠镁铝的密度逐渐增大,即Na<Mg<Al,故C错误;
D、通常金属越活泼,则硬度越小,故硬度Mg>K,故D错误.
故选B.
点评 本题考查金属性与非金属性的比较方法、密度的大小比较和硬度的大小比较,明确元素周期律是解本题的关键,注意总结规律,难度不大.

练习册系列答案
相关题目
10.分析下列合成路线: 则B物质应为下列哪种物质( )
则B物质应为下列哪种物质( )
 则B物质应为下列哪种物质( )
则B物质应为下列哪种物质( )| A. |  | B. |  | C. |  | D. |  |
13.某未知溶液中加入NaOH溶液并加热,有刺激性气味的气体氨气产生,说明溶液中有( )
| A. | Fe3+ | B. | NH4+ | C. | Cl- | D. | SO42- |
20.下列有关化学用语的表达正确的是( )
| A. | 甲醛的电子式: | B. | TNT 结构简式: | ||
| C. | 乙醛的结构简式为:CH3CHO | D. | 1,3-二甲基丁烷: |
10.下列有关表示正确的是( )
| A. | 过氧化钙(CaO2)的电子式: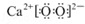 | |
| B. | 某微粒的结构示意简图为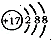 ,则该元素在周期表中位于第三周期、VIA族 ,则该元素在周期表中位于第三周期、VIA族 | |
| C. | H2CO3的电离方程式:H2CO3?2H++CO32- | |
| D. | 葡萄糖的结构简式:C6H12O6 |
17.下列实验操作对应的结论正确的是( )
| 选项 | 试验操作 | 结论 |
| A | 向NH4HSO4溶液中加入NaOH溶液至中性 | c(Na+)>c(SO42-)>c(NH4+) |
| B | 常温下将铝片插入浓硝酸中无明显变化 | 浓硝酸与铝片不反应 |
| C | 向鸡蛋清溶液中加入浓的(NH4)2SO4溶液,析出白色物质 | 蛋白质发生变性而聚沉 |
| D | 某溶液含有相同浓度的Cl-和CrO42-,逐滴加入AgNO3溶液,已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12 | CrO42-先沉淀 |
| A. | A | B. | B | C. | C | D. | D |
14.下列有关Na2CO3和NaHCO3性质的比较中,正确的是( )
| A. | 热稳定性:Na2CO3<NaHCO3 | |
| B. | 与相同浓度盐酸反应的快慢:Na2CO3>NaHCO3 | |
| C. | 106gNa2CO3和84gNaHCO3分别与过量盐酸反应,放出CO2质量:Na2CO3>NaHCO3 | |
| D. | Na2CO3 和NaHCO3均可与澄清石灰水反应 |
15.下列说法正确的是( )
| A. | 玻璃仪器都可以用于加热,但有些可以直接加热,有些需要垫上石棉网加热 | |
| B. | 给试管中的液体加热时,试管口不准对着别人,但可以对着自己 | |
| C. | 用H2还原氧化铜的实验中,应把H2通过预先加热的氧化铜 | |
| D. | 无论给试管中的液体还是固体加热,都必须先预热 |