题目内容
7.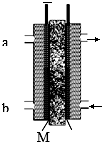 甲醇是燃料电池的常见原料,现以熔融的K2CO3为电解质,以甲醇为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.图是甲醇燃料电池模型,试回答下列问题:
甲醇是燃料电池的常见原料,现以熔融的K2CO3为电解质,以甲醇为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.图是甲醇燃料电池模型,试回答下列问题:①写出该燃料电池的正极反应式O2+4e-+2CO2=2CO32-.
②b处应该通入甲醇(填空气或者甲醇)M、N是阴离子交换膜,则阴离子移动的方向是从右到左(填“从左到右”或“从右到左”)
③用该电池电解500mL,0.2mol/L的CuSO4溶液,消耗3.2g甲醇时,阴极析出Cu的质量为6.4g.
分析 ①正极上氧气得到电子和二氧化碳反应生成碳酸根;
②甲醇在负极失电子,b侧通入,电解质中阴离子向负极移动;
③根据甲醇和转移电子之间的关系式计算转移电子的物质的量,再计算质量.
解答 解:①正极上氧气得到电子和二氧化碳反应生成碳酸根,电极反应为O2+4e-+2CO2=2CO32-,
故答案为:O2+4e-+2CO2=2CO32-;
②根据图片知,甲醇在负极失电子,b侧通入,M、N是离子交换膜,只能阴离子通过,碳酸根离子在负极上发生反应,所以碳酸根离子从右向左移动,
故答案为:甲醇;从右到左;
③根据CH3OH-6e-+3CO32-=4CO2+2H2O知,当有3.2g甲醇发生反应时转移电子的物质的量0.6mol,CuSO4只有0.1mol,转移0.2mol电子时已经消耗完毕,析出Cu的质量为6.4g.
故答案为:6.4g.
点评 本题考查了化学电源新型电池,从电极反应式、离子移动方向、物质的量的计算等方面考查,正确理解原电池原理即可解答,难点是电极反应式的书写,书写时要结合电解质特点.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
19.NA表示阿伏加德罗常数的值,下列说正确的( )
| A. | 17g氨气中所含质子数为10NA | |
| B. | 2.4g金属镁变成镁离子时失去电子数为0.1NA | |
| C. | 在标准状况下,22.4L氧气中所含的氧原子数为NA | |
| D. | 在25℃、压强为1.01×105Pa时,28g氮气所含的分子数为NA |
2.给定条件下,下列选项中所示的物质间转化均不能一步实现的是( )
| A. | 粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$Si | |
| B. | Mg(OH)2$\stackrel{盐酸}{→}$MgCl2 $\stackrel{电解}{→}$Mg | |
| C. | Na$→_{△}^{O_{2}}$Na2O2$\stackrel{H_{2}O}{→}$NaOH | |
| D. | AgNO3(aq)$\stackrel{NH_{3}•H_{2}O}{→}$[Ag(NH3)2]OH(aq)$\stackrel{蔗糖△}{→}$Ag |
12.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1 mol OH-中含有9NA个电子 | |
| B. | 28 g CO气体中含有NA个氧原子 | |
| C. | 1 mol/L AlCl3溶液中含有NA个Al3+ | |
| D. | 常温常压下,11.2 L甲烷气体中含有的分子数为0.5NA |
19.卤化物和卤酸盐在工业生产中有着重要的作用.某小组为探究其中一些盐的性质,查阅资料并进行实验.查阅资料如下:
①BrO3-+6I-+6H+=3I2+Br-+3H2O ②2BrO3-+I2=2IO3-+Br2
③IO3-+5I-+6H+=3I2+3H2O ④2IO3-+10Br-+12H+=I2+5Br2+6H2O
实验如下:
请回答:
(1)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是BrO3->IO3->Br2>I2;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是BrO3-+5Br-+6H+=3Br2+3H2O.
(2)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在下图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标).

①BrO3-+6I-+6H+=3I2+Br-+3H2O ②2BrO3-+I2=2IO3-+Br2
③IO3-+5I-+6H+=3I2+3H2O ④2IO3-+10Br-+12H+=I2+5Br2+6H2O
实验如下:
| 步骤 | 现象 |
| ⅰ.向盛有30mL 0.2mol•L-1 KI溶液的锥形瓶中依次 滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液 | 随着KBrO3溶液滴入,溶液由无色变为 蓝色并逐渐加深,最终保持不变 |
| ⅱ.继续向上述溶液中滴入KBrO3溶液 | 溶液的蓝色逐渐褪去 |
(1)根据资料中的反应①~④并结合所学知识,判断IO3-、BrO3-、I2、Br2的氧化性由强到弱的顺序是BrO3->IO3->Br2>I2;KBrO3溶液与KBr溶液在酸性条件下反应的离子方程式是BrO3-+5Br-+6H+=3Br2+3H2O.
(2)若用y表示锥形瓶中含碘物质的物质的量,用x表示所滴入KBrO3的物质的量,在下图中画出上述整个实验过程中y随x的变化曲线(要求:在图中标出终点坐标).

16.下列除去杂质的方法正确的是( )
| A. | 除去乙烷中少量的乙烯:催化条件下通入H2 | |
| B. | 除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液、干燥、蒸馏 | |
| C. | 除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶 | |
| D. | 除去乙醇中少量的乙酸:加足量生石灰、蒸馏 |
17.下列各物质中,按熔点由高到低的顺序排列的是( )
| A. | H2Te>H2Se>H2S>H2O | B. | KCl>NaCl>LiCl>HCl | ||
| C. | Sr>Ba>Ca>Be | D. | 金刚石>SiC>晶体硅 |
