题目内容
2.给定条件下,下列选项中所示的物质间转化均不能一步实现的是( )| A. | 粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$Si | |
| B. | Mg(OH)2$\stackrel{盐酸}{→}$MgCl2 $\stackrel{电解}{→}$Mg | |
| C. | Na$→_{△}^{O_{2}}$Na2O2$\stackrel{H_{2}O}{→}$NaOH | |
| D. | AgNO3(aq)$\stackrel{NH_{3}•H_{2}O}{→}$[Ag(NH3)2]OH(aq)$\stackrel{蔗糖△}{→}$Ag |
分析 A.硅与氯气反应生成四氯化硅,四氯化硅与氢气反应生成硅和氯化氢;
B.氢氧化镁与盐酸反应生成氯化镁,电解熔融氯化镁生成镁;
C.钠燃烧生成过氧化钠,过氧化钠与水反应生成氢氧化钠;
D.蔗糖为非还原性糖,不含醛基.
解答 解:A.硅与氯气反应生成四氯化硅,四氯化硅与氢气反应生成硅和氯化氢,所以粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$Si可以一步实现,故A不选;
B.氢氧化镁与盐酸反应生成氯化镁,电解熔融氯化镁生成镁,所以Mg(OH)2$\stackrel{盐酸}{→}$MgCl2 $\stackrel{电解}{→}$Mg可以一步实现,故B不选;
C.钠燃烧生成过氧化钠,过氧化钠与水反应生成氢氧化钠,所以Na$→_{△}^{O_{2}}$Na2O2$\stackrel{H_{2}O}{→}$NaoH可以一步实现,故C不选;
D.蔗糖为非还原性糖,不含醛基,不能还原银氨溶液,所以Ag(NH3)2]OH(aq)$→_{△}^{蔗糖}$Ag不能一步实现,故D选;
故选:D.
点评 本题考查了物质之间的转化,明确物质的性质是解题关键,注意蔗糖的结构特点,题目难度不大.

练习册系列答案
相关题目
13.将一定量的Na2CO3•10H2O与NaHCO3的混合物完全溶解于水,配成100mL溶液,测得溶液中Na+的浓度为0.4mol/L,若将溶液蒸干并灼烧到质量不变,可得到固体的质量是( )
| A. | 0.92g | B. | 1.68g | C. | 2.12g | D. | 2.55g |
14. 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )| A. | 最简单氢化物的稳定性:R>Q>X;R>T>X | |
| B. | 五种元素中Z的活动性最弱,T的氧化物对应水化合物酸性最强 | |
| C. | Q单质能从溶液中置换出X单质,R单质能从溶液中置换出T单质 | |
| D. | X阴离子和T阴离子相比,半径:X阴离子的大;还原性:T阴离子的强 |
11.已知:3H2+N2═2NH3为放热反应,对该反应的下列说法中正确的是( )
| A. | N2和H2的总能量一定大于NH3的总能量 | |
| B. | 因该反应为放热反应,故不必加热就可发生 | |
| C. | N2和H2的总能量一定低于NH3的总能量 | |
| D. | NH3的能量一定高于N2的能量 |
14.煤炭燃烧中会产生大量烟气容易造成污染,用如图所示的电解池在较高温度下反应,可以净化烟气,则下列判断不正确的是( )


| A. | 据图可知,阳极反应式为2SO42--4e-=2SO3↑+O2↑ | |
| B. | 阳极失去2mol电子时,理论上可以得到11.2L氧气 | |
| C. | SO2在阴极与O2反应生成硫酸根,则方程式为SO2+O2+2e-=SO42- | |
| D. | CO2不参与电极反应,净化器中CO2浓度升高 |
11.含有6.02×1023个O原子的H2O2物质的量是( )
| A. | 1mol | B. | 0.5mol | C. | 0.25mol | D. | 0.125mol |
12.下列各组中的两种物质在溶液中的反应,可用同一种离子方程式表示的是( )
| A. | 氧化铜分别溶于盐酸和醋酸 | |
| B. | 石灰石分别与硝酸和盐酸反应 | |
| C. | 硫酸铜溶液分别与氯化钡和氢氧化钡溶液反应 | |
| D. | 稀硫酸分别与碳酸钠、碳酸氢钠溶液反应 |
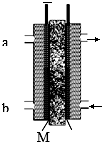 甲醇是燃料电池的常见原料,现以熔融的K2CO3为电解质,以甲醇为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.图是甲醇燃料电池模型,试回答下列问题:
甲醇是燃料电池的常见原料,现以熔融的K2CO3为电解质,以甲醇为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.图是甲醇燃料电池模型,试回答下列问题: