题目内容
下列气体的制备和性质实验中,由现象得出的结论错误的是
选项 | 试剂 | 试纸或试液 | 现象 | 结论 |
A | 亚硫酸钠、硫酸 | 品红试液 | 褪色 | SO2具有还原性 |
B | 浓盐酸、浓硫酸 | pH试纸 | 变红 | HCl为酸性气体 |
C | 浓盐酸、二氧化锰 | 淀粉碘化钾试液 | 变蓝 | Cl2具有氧化性 |
D | 浓氨水、生石灰 | 红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.白铁皮(镀锌)发生析氢腐蚀时,若转移0.2mol电子,下列说法正确的是( )
| A. | 有6.5 g锌被腐蚀 | B. | 有22.4 L氢气放出 | ||
| C. | 有2.8 g铁被腐蚀 | D. | 有2.24 L氢气放出 |
12.废铅蓄电池量急速增加所引起的铅污染日益严重.工业上从废铅蓄电池的铅膏回收铅的工艺流程如下:
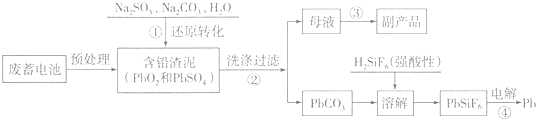
已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14.
回答下列问题:
(1)写出步骤①中PbSO4转化为PbCO3过程的平衡常数表达式K=$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$,为提高步骤①的反应速率和铅浸出率,你认为可采取的两条措施是充分搅拌、适当升高温度.
(2)步骤①中发生的氧化还原反应的离子方程式为PbO2+SO32-+H2O=PbSO4+2OH-.
(3)写出步骤④用惰性电极电解的阴极反应式Pb2++2e-=Pb.
(4)PbO2在加热过程发生分解的失重曲线如图1所示,已知失重曲线上的a点为样品失重4.0%(即$\frac{样品起始质量-a点固体质量}{样品起始质量}$×100%)的残留固体,若a点固体组成表示为PbOx,计算x=1.4.
(5)铅的加工同样会使水体中重金属铅的含量增大造成严重污染.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-.各形态的浓度分数α随溶液pH变化的关系如图2所示,某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如表
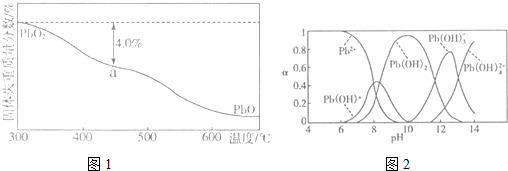
则上表中除Pb2+外,该脱铅剂对其他离子的去除效果最好的是Fe3+,如果该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:2EH(s)+Pb2+?E2Pb(s)+2H+.则脱铅的最合适pH范围为B(填字母).
A.4~5 B.6~7 C.9~10 D.11~12.

已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14.
回答下列问题:
(1)写出步骤①中PbSO4转化为PbCO3过程的平衡常数表达式K=$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$,为提高步骤①的反应速率和铅浸出率,你认为可采取的两条措施是充分搅拌、适当升高温度.
(2)步骤①中发生的氧化还原反应的离子方程式为PbO2+SO32-+H2O=PbSO4+2OH-.
(3)写出步骤④用惰性电极电解的阴极反应式Pb2++2e-=Pb.
(4)PbO2在加热过程发生分解的失重曲线如图1所示,已知失重曲线上的a点为样品失重4.0%(即$\frac{样品起始质量-a点固体质量}{样品起始质量}$×100%)的残留固体,若a点固体组成表示为PbOx,计算x=1.4.
(5)铅的加工同样会使水体中重金属铅的含量增大造成严重污染.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-.各形态的浓度分数α随溶液pH变化的关系如图2所示,某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如表

| 离子/(mol.L-1) | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度 | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度 | 0.004 | 22.6 | 0.040 | 0.053 | 49.9 |
A.4~5 B.6~7 C.9~10 D.11~12.