题目内容
1.根据有关信息,写出符合要求的离子方程式(1)化学在环境保护中起着十分重要的作用,催化反硝化法可用于治理水中硝酸盐的污染.催化反硝化法中,H2能将NO3-还原为N2.上述反应的离子方程式为2NO3-+5H2$\frac{\underline{\;催化剂\;}}{\;}$N2+2OH-+4H2O.
(2)利用I2的氧化性可测定钢铁中硫的含量.做法是将钢样中的硫转化成H2SO3,然后用一定浓度的I2溶液进行滴定,滴定反应的离子方程式为H2SO3+I2+H2O=4H++SO42-+2I-.
(3)某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等,正极材料可再生利用,其中一步工艺流程为用氢氧化钠溶液进行“正极碱浸”,发生反应的离子方程式2Al+2OH-+6H2O=2Al(OH)-4+3H2↑
(4)Fe的一种含氧酸根FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生.该反应的离子方程式是4FeO42-+20H+=4Fe3++3O2↑+10H2O.
分析 (1)根据信息:用H2将NO3-还原为N2,一段时间后,溶液的碱性明显增强,即生成氢氧根离子,据此书写方程式;
(2)碘单质将亚硫酸氧化成硫酸,据此写出反应的离子方程式;
(3)正极材料为铝与氢氧化钠溶液,二者反应生成偏铝酸钠和氢气;
(4)FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,说明有Fe3+生成,并有无色气体产生,根据电子转移守恒,只能为O元素被氧化,故还生成O2,配平书写离子方程式.
解答 解:(1)根据信息:用H2将NO3-还原为N2,一段时间后,溶液的碱性明显增强,即生成氢氧根离子,发生的反应为:2NO3-+5H2$\frac{\underline{\;催化剂\;}}{\;}$N2+2OH-+4H2O,
故答案为:2NO3-+5H2$\frac{\underline{\;催化剂\;}}{\;}$N2+2OH-+4H2O;
(2)碘单质与亚硫酸发生氧化还原反应,反应的离子方程式为:H2SO3+I2+H2O=4H++SO42-+2I-,
故答案为:H2SO3+I2+H2O=4H++SO42-+2I-;
(3)锂离子电池正极材料中只有铝箔与氢氧化钠反应,发生反应的离子方程式:2Al+2OH-+6H2O=2Al(OH)4-+3H2↑,
故答案为:2Al+2OH-+6H2O=2Al(OH)4-+3H2↑;
(4)FeO42-具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,说明有Fe3+生成,并有无色气体产生,根据电子转移守恒,只能为O元素被氧化,故还生成O2,反应离子方程式为:4FeO42-+20H+=4Fe3++3O2↑+10H2O,
故答案为:4FeO42-+20H+=4Fe3++3O2↑+10H2O.
点评 本题考查了离子方程式的书写,题目难度中等,明确离子方程式的书写原则为解答关键,注意掌握常见元素及其化合物性质,试题培养了学生的分析能力及灵活应用基础知识的能力.

 天天练口算系列答案
天天练口算系列答案| A. | 淀粉、纤维素和蔗糖都属于糖类 | |
| B. | 麦芽糖和葡萄糖都属于单糖,不能再进一步水解 | |
| C. | 可以用新制的氢氧化铜检验病人尿液中是否含有葡萄糖 | |
| D. | 油脂是高级脂肪酸的甘油酯 |
| X | Y | Z |
| W | ||
| T |
| A. | 单质X2与Y2在放电作用下不能直接反应得到XY2 | |
| B. | X2Y2易溶于H2Y是由于它们分子间存在氢键的缘故 | |
| C. | 非金属性:Z元素比W元素强;酸性:HZ比HW强 | |
| D. | TY2既具有氧化性,也具有还原性 |
| A. | 甲烷和乙烯 | B. | 乙烷和苯(C6H6) | ||
| C. | 丁烷和2-甲基丙烷 | D. | 苯和甲苯(C6H5CH3) |
(1)测量前,应把天平放在水平台上,当移动游码至零刻度处时,指针偏向分度盘的右侧,则应将平衡螺母向左调,使指针指在分度盘的中央.
(2)接下来的测量步骤如下:
①往烧杯中倒入适量的硫酸铜溶液,测出烧杯和溶液的质量为49.2g;
②将烧杯中的一部分溶液倒入量筒,读出量筒中溶液的体积为20mL;
③测出烧杯和剩余溶液的质量,砝码及游码的位置如图所示.
将下面的实验记录表填写完整:
| 烧杯和溶液的质量/g | 烧杯和剩余溶液的质量/g | 量筒中溶液的质量/g | 量筒中溶液的体积/cm3 | 硫酸铜溶液的密度ρ/(g•cm-3) |
| 49.2 | 28.2 | 21 | 20 | 1.05 |
因为物体悬浮时,V物=V排,
所以:ρ物=ρ液,即血液的密度等于硫酸铜溶液的密度.
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式:___________.
(2)实验室用两种固体制取NH3的反应化学方程式为_____________.
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为_____________.
(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为_____________.
(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:
T/℃ | 165 | 175 | 185 | 195 |
K | 111.9 | 74.1 | 50.6 | 34.8 |
①焓变△H_________0(填“>”、“<”或“=”).
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)\frac{n(NH_{3})}{n(CO_{2})}=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是_____________.图中A点处,NH3的平衡转化率为___________.

(6)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:N2(g)+3H2(g)?2NH3(g),测得甲容器中H2的平衡转化率为40%.
n(N2) | n(H2) | n(NH3) | |
甲 | 1mol | 3mol | 0mol |
乙 | 0.5mol | 1.5mol | 1mol |
丙 | 0mol | 0mol | 4mol |
①判断乙容器中反应进行的方向是_____________(填“正向或“逆向”)移动.
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为_____________。
(6)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式: ,科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是 (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为 。
(7)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是 (填字母代号)。
4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是 (填字母代号)。
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(8)如果某氨水的电离程度为1%,浓度为0.01 mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3·H2O的浓度为 {已知Ksp[Mg(OH)2]=4.0×10-12]}
下列气体的制备和性质实验中,由现象得出的结论错误的是
选项 | 试剂 | 试纸或试液 | 现象 | 结论 |
A | 亚硫酸钠、硫酸 | 品红试液 | 褪色 | SO2具有还原性 |
B | 浓盐酸、浓硫酸 | pH试纸 | 变红 | HCl为酸性气体 |
C | 浓盐酸、二氧化锰 | 淀粉碘化钾试液 | 变蓝 | Cl2具有氧化性 |
D | 浓氨水、生石灰 | 红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
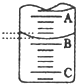
(2)如图表示50mL,滴定管中液面的位置,若A与C刻度间相差1mL,
A处的刻度为25,滴定管中液面读数应为25.40mL.,此时滴定管中液体的体积大于24.60mL.
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准漓浓度为c mol•L-1,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.32 | 25.28 |
A.实验结束时俯视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
E.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)根据所给数据,写出计算该白醋中总酸度的表达式(不必化简):$\frac{\frac{25.28+25.32}{2}×c×0.1×60}{2V}$.