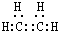题目内容
6.下列物质的水溶液因水解呈酸性的是( )| A. | NaOH | B. | Na2CO3 | C. | NH4Cl | D. | HCl |
分析 因发生水解而显酸性的物质为强酸弱碱盐,弱碱阳离子结合水电离出的氢氧根离子促进了水的电离,溶液氢氧根离子浓度大于氢离子浓度,溶液呈酸性,据此进行解答.
解答 解:A.NaOH为强碱,其溶液呈碱性,故A不选;
B.Na2CO3为强碱弱酸盐,碳酸根离子水解呈碱性,故B不选;
C.NH4Cl为强酸弱碱盐,铵根离子发生水解呈酸性,故C选;
D.HCl为一元强酸,在溶液中电离子出氢离子,溶液呈酸性,不是水解的原因,故D不选;
故选C.
点评 本题考查盐类水解的应用,题目难度不大,明确盐类水解的规律以及水解原理为解答关键,试题有利于提高学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
16.下列不能证明一元酸HA为弱酸的是( )
| A. | NaA溶液的pH>7(室温下) | |
| B. | pH试纸显示0.1 mol/L HA溶液的pH为2~3(室温下) | |
| C. | 0.1 mol/L的HCl和HA溶液,前者的导电能力明显更强 | |
| D. | HA溶液能与CH3COONa溶液反应生成CH3COOH |
1.设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | NA个N2分子与NA个CO分子的质量比为1﹕1 | |
| B. | 水的摩尔质量等于NA个水分子的质量 | |
| C. | 在常温常压下,11.2LSO2含有的分子数为0.5NA | |
| D. | 1L 0.1mol•L-1Na2SO4溶液中有0.1NA个Na+ |
16.某种煤气的主要成分是CO、H2,把一套以煤气为燃料的灶具改为以天然气为燃料的灶具时,灶具应作相应的调整,正确的方法是( )
| A. | 空气和天然气的进人量都减少 | |
| B. | 减小天然气的进人童或增大空气的进入量 | |
| C. | 空气和天然气的进人童都增大 | |
| D. | 增大天然气的进人量或减小空气的进入量 |
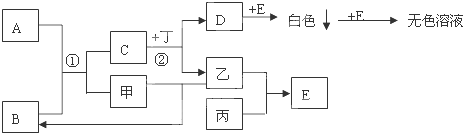
 已知气态烃A是一种基本的有机化工原料,目前石油裂解已成为生成A的主要方法.A在标准状况下的密度为1.25g•L-1.A、B、C、D在一定条件下存在如下转化关系(反应条件、部分产物被省略).请回答下列问题:
已知气态烃A是一种基本的有机化工原料,目前石油裂解已成为生成A的主要方法.A在标准状况下的密度为1.25g•L-1.A、B、C、D在一定条件下存在如下转化关系(反应条件、部分产物被省略).请回答下列问题: