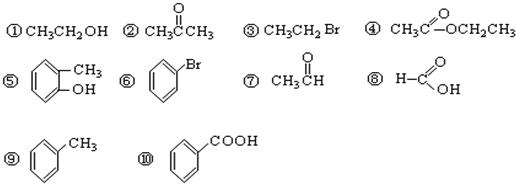
题目内容
11. 已知气态烃A是一种基本的有机化工原料,目前石油裂解已成为生成A的主要方法.A在标准状况下的密度为1.25g•L-1.A、B、C、D在一定条件下存在如下转化关系(反应条件、部分产物被省略).请回答下列问题:
已知气态烃A是一种基本的有机化工原料,目前石油裂解已成为生成A的主要方法.A在标准状况下的密度为1.25g•L-1.A、B、C、D在一定条件下存在如下转化关系(反应条件、部分产物被省略).请回答下列问题:(1)有机物A的电子式是
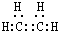
(2)B、C、D中含有的官能团的名称分别是羟基、醛基、羧基.
(3)反应②的化学方程式是2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,反应类型氧化反应.
反应④的化学方程式是CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,反应类型酯化或取代.
分析 石油裂解已成为生成A的主要方法,A在标准状况下的密度为1.25g•L-1,则A的相对分子质量为28,则A为CH2=CH2,A与水发生加成生成B为CH3CH2OH,B发生氧化反应生成C为CH3CHO,C发生氧化反应生成D为CH3COOH,B和D发生酯化反应生成CH3COOCH2CH3,据此答题.
解答 解:石油裂解已成为生成A的主要方法,A在标准状况下的密度为1.25g•L-1,则A的相对分子质量为28,则A为CH2=CH2,A与水发生加成生成B为CH3CH2OH,B发生氧化反应生成C为CH3CHO,C发生氧化反应生成D为CH3COOH,B和D发生酯化反应生成CH3COOCH2CH3,
(1)根据上面的分析可知,A为CH2=CH2,其电子式为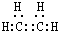 ,故答案为:
,故答案为: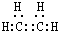 ;
;
(2)B为CH3CH2OH,C为CH3CHO,D为CH3COOH,所含的官能团依次为羟基、醛基、羧基,
故答案为:羟基、醛基、羧基;
(3)反应②是乙醇氧化成乙醛,反应的化学方程式是2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,反应类型是氧化反应,反应④是乙醇和乙酸发生酯化生成乙酸乙酯,反应的化学方程式是 CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,也属于取代反应,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;氧化反应;CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O;酯化或取代.
点评 本题考查有机物推断,涉及烯、醇、羧酸、酯的性质与转化等,难度不大,注意基础知识的理解掌握.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
1.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 0.1mol•L-1 稀硫酸中含有SO42-离子个数为0.1NA | |
| B. | 0.1molNa2O2与CO2完全反应,转移电子数为0.2 NA | |
| C. | 常温常压下,46 g的NO2和46g 的N2O4含有的原子数相等 | |
| D. | 标准状况下,22.4L SO3所含的分子数为NA |
2.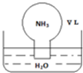 标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )
标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )
 标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )
标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )| A. | 条件不足,不能计算所得溶液的物质的量浓度 | |
| B. | 所得溶液中,n(NH3•H2O)+n(NH4+)+n(NH3)=$\frac{V}{22.4}$ | |
| C. | 所得溶液的质量分数为$\frac{17ρ}{22400}$ | |
| D. | 水最终不可能充满整个烧瓶 |
6.下列物质的水溶液因水解呈酸性的是( )
| A. | NaOH | B. | Na2CO3 | C. | NH4Cl | D. | HCl |
1.用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A. | 6g SiO2所含分子数为0.1NA,化学键总数为0.4NA | |
| B. | 将2mL 0.5mol/L Na2SiO3溶液滴入稀盐酸中制得H2SiO3胶体,所含胶粒数为0.001NA | |
| C. | 常温常压下,32gO2和O3的混合气体中含有的氧原子数为2NA | |
| D. | 25℃时,PH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |