题目内容
若向B、D、F三支试管中分别加入等量的碘液,观察三支试管,发现液体的颜色是蓝色,产生该颜色的原因是( )
| A、淀粉完全水解 |
| B、淀粉部分水解 |
| C、淀粉未能水解 |
| D、淀粉酶与碘反应 |
考点:淀粉的性质和用途
专题:有机反应
分析:淀粉与碘液作用显示蓝色,据此解题.
解答:
解:淀粉与碘液作用显蓝色,若向B、D、F三支试管中分别加入等量的碘液,发现液体的颜色是蓝色,B、D试管中剩余淀粉遇碘变蓝,说明淀粉部分水解,F试管中淀粉酶在100℃时失活,淀粉没有被分解,淀粉遇碘变蓝,
故选B.
故选B.
点评:本题主要考查了淀粉的检验,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.

练习册系列答案
相关题目
已知氟利昂的化学式为CCl2F2,则沸点不同的氟利昂有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
下列各电子式中正确的是( )
A、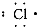 氯原子 |
B、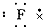 氟原子 |
C、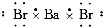 溴化钡 |
D、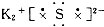 硫化钾 |
液体颜色不呈砖红色的原因是( )
| A、淀粉酶在40℃时活性相对较高 |
| B、淀粉酶催化淀粉水解产生的无还原糖 |
| C、淀粉酶与新制氢氧化铜反应 |
| D、淀粉酶在100℃时失活 |
下列各组离子在指定溶液中,能大量共存的是( )
①无色溶液中:K+、Na+、MnO4-、SO42-
②pH=13的溶液中:CO32-、Na+、AlO2-、NO3-
③由水电离出的c(H+)=10-12 mol/L的溶液:Ba2+、Na+、NO3-、Cl-
④强酸性溶液中:Fe3+、NO3-、Na+、SO42-
⑤强酸性溶液中:Fe2+、Al3+、NO3-、Cl-.
①无色溶液中:K+、Na+、MnO4-、SO42-
②pH=13的溶液中:CO32-、Na+、AlO2-、NO3-
③由水电离出的c(H+)=10-12 mol/L的溶液:Ba2+、Na+、NO3-、Cl-
④强酸性溶液中:Fe3+、NO3-、Na+、SO42-
⑤强酸性溶液中:Fe2+、Al3+、NO3-、Cl-.
| A、②③④ | B、②④⑤ |
| C、①②⑤ | D、②④ |
已知在101kPa时:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-820kJ?mol-1.则下列说法正确的是( )
| A、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H>-820 kJ?mol-1 |
| B、CH4的燃烧热是820kJ?mol-1 |
| C、1mol CH4和2mol O2的键能之和大于1mol CO2和2mol H2O的键能之和 |
| D、11.2L(标准状况)CH4完全燃烧生成气态水时放出410kJ热量 |
下列有关电池的叙述正确的是( )
| A、锌锰干电池工作一段时间后碳棒变细 |
| B、最早使用的充电电池是锌锰电池 |
| C、锂离子电池是新一代可充电的绿色电池 |
| D、太阳能电池的主要材料是高纯度的二氧化硅 |
若图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池,则下列的说法中正确的是( )


| A、图2电池在放电过程中,正极区的电极反应为:BH4--8e-+8OH-═BO2-+6H2O |
| B、若用稀硫酸浸湿滤纸并用导线将a、b相连,则有电子从b极流出通过导线流向a极 |
| C、若用硫酸钠和紫色石蕊的混合溶液浸湿滤纸并用导线将a、b相连,则可看到铅笔芯C点处浸有紫色石蕊的滤纸变蓝,此处发生电极反应为:O2+2H2O+4e-═4OH- |
| D、若用KI-淀粉溶液浸湿滤纸,同时用导线将a、b分别与A、B电极相连,若看到铅笔芯C点处出现变蓝现象,则b极连接的是燃料电池的A极 |
下列各组气体,不论以何种比例混合,同温、同压时,其密度不等于N2的密度的是( )
| A、O2和H2 |
| B、C2H4和CO |
| C、CH4和C3H6 |
| D、O2和Cl2 |