题目内容
20.根据下列实验操作和现象所得出的结论不正确的是( )| 实验操作 | 实验现象 | 结论 | |
| A | 向硅酸钠溶液中滴加1滴酚酞,再逐滴加入稀盐酸至红色褪去 | 试管里出现白色沉淀 | 酸性:盐酸>硅酸 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化但不滴落 | 熔点:氧化铝>铝 |
| C | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 该溶液中一定含有SO42- |
| D | 向某无色溶液中先滴加氯水,再加少量CCl4,振荡,静置 | 溶液分层,下层为橙红色 | 溶液中含有Br- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.发生强酸制取弱酸的反应,白色沉淀为硅酸;
B.氧化铝的熔点高,包裹在Al的外面;
C.白色沉淀可能为AgCl或BaSO4;
D.溶液分层,下层为橙红色,可知氯水氧化溴离子生成溴.
解答 解:A.发生强酸制取弱酸的反应,白色沉淀为硅酸,则酸性:盐酸>硅酸,故A正确;
B.氧化铝的熔点高,包裹在Al的外面,则铝箔熔化但不滴落,熔点:氧化铝>铝,故B正确;
C.白色沉淀可能为AgCl或BaSO4,则该溶液中可能含有SO42-,故C错误;
D.溶液分层,下层为橙红色,可知氯水氧化溴离子生成溴,则溶液中含有Br-,故D正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握酸性比较、离子检验、物质的性质、实验技能为解答关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案
相关题目
11.下列分子中属于含极性键的非极性分子的是( )
| A. | Cl2 | B. | CS2 | C. | CCl4 | D. | NH3 |
8.下列实验中,对应的现象以及结论都正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A. | 将过量稀盐酸加入铁粉中,充分反应 | 有气体生成,溶液呈黄色 | 稀盐酸将Fe氧化为Fe3+ |
| B. | 将铜粉加1.0mol•L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D. | 把一小块钠放在坩埚里加热 | 钠先熔化,发出黄色火焰最后生成淡黄色固体 | 生成了Na2O2 |
| A. | A | B. | B | C. | C | D. | D |
15.下列有关实验的说法正确的是( )
| A. | 做蒸馏实验时,如果加热后发现忘记加沸石,应停止加热,冷却后补加 | |
| B. | 氨气可使湿润的蓝色石蕊试纸变红 | |
| C. | 用稀硝酸除去Cu中混有的CuO | |
| D. | 向某溶液中滴加氯水后再滴加KSCN溶液,溶液变红说明原溶液一定含有Fe2+ |
12.下列实验能成功的是( )
| A. | 用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热 | |
| B. | 苯和浓溴水反应制溴苯 | |
| C. | CH3CH2Br中加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 | |
| D. | 将乙酸和乙醇混合加热制乙酸乙酯 |
10.下列叙述中,不正确的是( )
| A. | 漂白粉的有效成分是氯化钠 | B. | 氯水中的次氯酸具有杀菌消毒作用 | ||
| C. | 过氧化钠可用作潜艇里氧气的来源 | D. | 食醋可用于清除暖水瓶中的水垢 |
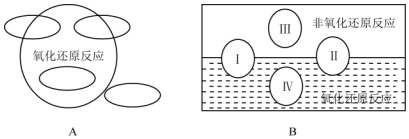 氧化还原是常见的反应类型,根据信息回答以下问题:
氧化还原是常见的反应类型,根据信息回答以下问题: