题目内容
17.短周期元素X、Y、Z、W、Q在元素周期表中的位置如下表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法不正确的是( )| X | Y | ||||
| Z | W | Q |
| A. | Y与Z的简单离子的半径大小关系为Y2->Z2+ | |
| B. | Z单质可以在X和Y组成的化合物中燃烧 | |
| C. | W与Y组成的某种化合物是光导纤维的主要成分 | |
| D. | Q单质具有强氧化性和漂白性 |
分析 X元素原子的内层电子数是最外层电子数的一半,X原子只能有2个电子层,最外层电子数为4,则X为碳元素;由元素在周期表中的位置可知,Y为O、Z为Mg、W为Si、Q为Cl,以此解答该题.
解答 解:X元素原子的内层电子数是最外层电子数的一半,X原子只能有2个电子层,最外层电子数为4,则X为碳元素;由元素在周期表中位置可知,Y为O、Z为Mg、W为Si、Q为Cl,
A.Y与Z的简单离子分别是O2-、Mg2+,电子层结构相同,序小半径反而大,则Y2->Z2+,故A正确;
B.Z单质是镁,可以在X和Y组成的化合物二氧化碳中燃烧生成氧化镁和碳,故B正确;
C.W与Y组成二氧化硅,二氧化硅是光导纤维的主要成分,故C正确;
D.干燥的氯气没有漂白性,故D错误;
故选:D.
点评 本题考查结构性质位置关系应用,为高频考点,确定X是解题关键,注意掌握元素周期表的结构及元素周期律,难度不大.

练习册系列答案
相关题目
8.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1L 0.1mol/L的NaHS溶液中HS-和S2-离子数之和为0.1NA | |
| B. | 3 mol Fe在足量的水蒸气中完全反应转移9NA个电子 | |
| C. | 2.0 g H218O与D2O的混合物中所含中子数为NA | |
| D. | 1 mol Na2CO3晶体中含离子总数大于3NA |
12.化学来源于生活也服务于生活,下列关于生活中的化学叙述正确的是( )
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 用活性炭为蔗糖脱色和用臭氧漂白纸浆原理相似 | |
| C. | 雾霾是许多细小液体和固体微粒分散到空气中形成的一种气溶胶 | |
| D. | 光导纤维在信息领域应用越来越广泛,光导纤维的主要成分是Si单质 |
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| B. | 标准状况下,11.2LNO2气体含有的分子数为 NA | |
| C. | 将1mol FeCl3水解制成胶体,所得胶体中含有的胶体粒子数NA | |
| D. | 2.0gH218O与D2O的混合物中所含中子数为NA |
9.在反应3Fe3O4+28HNO3═9Fe(NO3)3+NO+14H2O中,还原剂和氧化剂的物质的量之比是( )
| A. | 3:28 | B. | 3:1 | C. | 9:28 | D. | 1:3 |
6.下列有关实验操作、现象、解释和结论都正确的是( )
| 选项 | 操 作 | 现 象 | 解释、结论 |
| A | 用玻璃棒蘸取浓氨水点到干燥红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了Na2CO3晶体 |
| C | 向蔗糖中加入浓硫酸并搅拌 | 蔗糖变黑,体积膨胀 | 反应中浓硫酸只体现脱水性 |
| D | 过量的Fe粉与氯气充分反应后,向反应后的混合物中加水,取上层清液滴入KSCN溶液 | 溶液不变红色 | 氯气将Fe氧化为Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
7.化学与我们的生活息息相关.下列说法不正确的是( )
| A. | 玻璃、水晶和陶瓷都是传统硅酸盐材料 | |
| B. | 可溶性铝盐和铁盐可用作净水剂 | |
| C. | SO2和NO都能形成酸雨而破坏环境 | |
| D. | CO2和CH4都是引起温室效应的气体 |
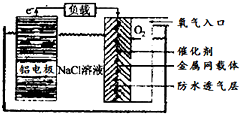 铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料.
铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料.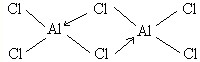 .
.
 ,写出该反应的化学方程式
,写出该反应的化学方程式 .
. )在POCl3(三氯氧磷)的催化下反应生成E,同时还生成H2O和另一种有机物,写出该有机物的分子式C2H7N.
)在POCl3(三氯氧磷)的催化下反应生成E,同时还生成H2O和另一种有机物,写出该有机物的分子式C2H7N. 或
或 .(写出其中一种的结构简式)
.(写出其中一种的结构简式) 和(CH3CO)2O为原料制备
和(CH3CO)2O为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: