题目内容
8.设NA为阿伏伽德罗常数的值,下列说法正确的是( )| A. | 1L 0.1mol/L的NaHS溶液中HS-和S2-离子数之和为0.1NA | |
| B. | 3 mol Fe在足量的水蒸气中完全反应转移9NA个电子 | |
| C. | 2.0 g H218O与D2O的混合物中所含中子数为NA | |
| D. | 1 mol Na2CO3晶体中含离子总数大于3NA |
分析 A、根据物料守恒来分析;
B、铁和水蒸气反应后变为+$\frac{8}{3}$价;
C、H218O与D2O的摩尔质量均为20g/mol,且两者均含10个中子;
D、碳酸钠晶体由2个钠离子和1个碳酸根构成.
解答 解:A、HS-是酸式弱酸根,在溶液中既能电离为S2-又能水解为H2S,根据物料守恒可知溶液中S2-、HS-和S2-之和为0.1NA个,故A错误;
B、铁和水蒸气反应后变为+$\frac{8}{3}$价,故3mol铁完全反应后转移8mol即8NA个电子,故B错误;
C、H218O与D2O的摩尔质量均为20g/mol,故2.0g混合物的物质的量为0.1mol,且两者均含10个中子,故0.1mol混合物中含NA个中子,故C正确;
D、碳酸钠晶体由2个钠离子和1个碳酸根构成,故1mol碳酸钠中含有3NA个离子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
19.在水中加入下列物质,可使水的电离平衡正向移动,且所得溶液呈酸性的是( )
| A. | NaCl | B. | H2SO4 | C. | Na2CO3 | D. | NH4Cl |
16.在pH=1的无色溶液中,下列各离子组因发生氧化还原反应而不能共存的是( )
| A. | NH4+ K+ Na+ CO32- NO3- | B. | K+ Na+ Fe2+ SO42- NO3- | ||
| C. | NH4+ K+ Na+ HCO3-Cl- | D. | NH4+ K+ Na+ NO3- I- |
3.A、B、C、D都是短周期元素,原子半径:D>C>A>B.已知A、B处在同一周期,A、C处在同一主族,C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层上的电子数是D原子最外层电子数的3倍.下列说法中正确的是( )
| A. | 简单离子半径:D>B | |
| B. | 气态氢化物的稳定性:A>B | |
| C. | B、D两元素可组成阴、阳离子个数比为1:1的化合物 | |
| D. | B、C、D三种元素可组成化学式为DCB2的化合物,其水溶液显碱性 |
13.化学离不开生活,生活也离不开化学.下列叙述中科学的是( )
| A. | 广告语“农家肥蔬菜,无公害,绝对不含任何化学物质” | |
| B. | 医用酒精是利用了乙醇的氧化性来杀菌消毒的 | |
| C. | 面食加工时加入少量苏打粉时是防止酸败,加入少量小苏打粉时是作膨松剂 | |
| D. | 空气质量日报中计入污染指数的项目为可吸入颗粒物、SO2、NOx、CO2 |
20.早在古代,我国人民就积累了不少对化学物质变化的认识.例如,晋代炼丹家、医学家葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银,积变又成丹砂”.这句话中的丹砂指的是HgS,下列关于这句话的说法正确的是( )
| A. | 这个过程只涉及物理变化 | |
| B. | 这个过程是可逆反应 | |
| C. | 这个过程发生了复分解反应 | |
| D. | “丹砂烧之成水银”过程中还可能产生SO2 |
17.短周期元素X、Y、Z、W、Q在元素周期表中的位置如下表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法不正确的是( )
| X | Y | ||||
| Z | W | Q |
| A. | Y与Z的简单离子的半径大小关系为Y2->Z2+ | |
| B. | Z单质可以在X和Y组成的化合物中燃烧 | |
| C. | W与Y组成的某种化合物是光导纤维的主要成分 | |
| D. | Q单质具有强氧化性和漂白性 |
18.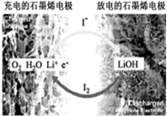 科学家开发出一种新型电池,其能量密度极高,效率达90%以上,电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O$?_{充电}^{放电}$2I2+4LiOH,对于该电池的下列说法不正确的是( )
科学家开发出一种新型电池,其能量密度极高,效率达90%以上,电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O$?_{充电}^{放电}$2I2+4LiOH,对于该电池的下列说法不正确的是( )
 科学家开发出一种新型电池,其能量密度极高,效率达90%以上,电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O$?_{充电}^{放电}$2I2+4LiOH,对于该电池的下列说法不正确的是( )
科学家开发出一种新型电池,其能量密度极高,效率达90%以上,电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O$?_{充电}^{放电}$2I2+4LiOH,对于该电池的下列说法不正确的是( )| A. | 充电时Li+从阳极区移向阴极区 | |
| B. | 充电时阴极反应为LiOH+e-═Li+OH- | |
| C. | 放电时负极上I-被氧化 | |
| D. | 放电时正极反应为O2+2H2O+4Li++4e-═4LiOH |