题目内容
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| B. | 标准状况下,11.2LNO2气体含有的分子数为 NA | |
| C. | 将1mol FeCl3水解制成胶体,所得胶体中含有的胶体粒子数NA | |
| D. | 2.0gH218O与D2O的混合物中所含中子数为NA |
分析 A、pH=13的氢氧化钡溶液中,氢氧根的浓度为0.1mol/L;
B、分子数N=$\frac{V}{Vm}{N}_{A}$;
C、一个胶粒是多个氢氧化铁的聚集体;
D、H218O与D2O的摩尔质量均为20g/mol,且均含10个中子.
解答 解:A、pH=13的氢氧化钡溶液中,氢氧根的浓度为0.1mol/L,故1L溶液中含有的氢氧根的个数为0.1NA个,故A错误;
B、分子数N=$\frac{V}{Vm}{N}_{A}$=$\frac{11.2L}{22.4L/mol}×{N}_{A}/mol$=0.5NA个,故B错误;
C、一个胶粒是多个氢氧化铁的聚集体,故1mol氯化铁形成的胶粒个数小于NA个,故C错误;
D、H218O与D2O的摩尔质量均为20g/mol,故2.0g混合物的物质的量为0.1mol,且;离两者均含10个中子,故0.1mol混合物中含NA个中子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
12.下列属于原子晶体的化合物是( )
| A. | 干冰 | B. | 二氧化硅 | C. | 金刚石 | D. | 氯化钠 |
13.化学离不开生活,生活也离不开化学.下列叙述中科学的是( )
| A. | 广告语“农家肥蔬菜,无公害,绝对不含任何化学物质” | |
| B. | 医用酒精是利用了乙醇的氧化性来杀菌消毒的 | |
| C. | 面食加工时加入少量苏打粉时是防止酸败,加入少量小苏打粉时是作膨松剂 | |
| D. | 空气质量日报中计入污染指数的项目为可吸入颗粒物、SO2、NOx、CO2 |
17.短周期元素X、Y、Z、W、Q在元素周期表中的位置如下表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法不正确的是( )
| X | Y | ||||
| Z | W | Q |
| A. | Y与Z的简单离子的半径大小关系为Y2->Z2+ | |
| B. | Z单质可以在X和Y组成的化合物中燃烧 | |
| C. | W与Y组成的某种化合物是光导纤维的主要成分 | |
| D. | Q单质具有强氧化性和漂白性 |
7.下列说法错误的是( )
| A. | 中子数为20的氯原子:${\;}_{17}^{37}$Cl | B. | 乙酸的分子式为:C2H4O2 | ||
| C. | 乙醛的结构简式:CH3COH | D. | 比例模型 可以表示CO2 分子 可以表示CO2 分子 |
14.下列对有关化工生产的说法正确的是( )
| A. | 合成氨生产过程中将NH3液化分离,可以提高反应物的转化率 | |
| B. | 硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 | |
| C. | 电解饱和食盐水制烧碱采用离子交换膜法,可防止阳极室产生的Cl2进入阴极室 | |
| D. | 传统硅酸盐工业中生产水泥的原料为石灰石、纯碱和石英砂 |
12.化学与社会、生活密切相关.下列现象或事实及对应解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 可用铁制容器储存、运输浓硫酸 | 常温下铁与浓硫酸不反应 |
| B | 可用二氧化硫漂白纸浆、草帽等 | 二氧化硫具有氧化性 |
| C | 可用碳酸钠溶液将水垢中的硫酸钙转化为碳酸钙 | Ksp(CaSO4)>Ksp(CaCO3) |
| D | 福尔马林常用来保存新鲜食品 | 福尔马林具有杀菌防腐性能 |
| A. | A | B. | B | C. | C | D. | D |
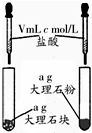
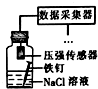
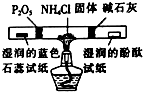
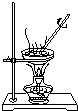
 如图各物质是中学化学中常见的物质,甲、乙均是离子化合物,且阴、阳离子个数比为1:1.甲是发酵粉的主要成分,乙是一种常用的化肥.B、D常温常压下是气体.请回答下列问题:
如图各物质是中学化学中常见的物质,甲、乙均是离子化合物,且阴、阳离子个数比为1:1.甲是发酵粉的主要成分,乙是一种常用的化肥.B、D常温常压下是气体.请回答下列问题: