题目内容
18.下列元素在自然界中仅以化合态存在的是( )①Si ②Al ③Cl ④Fe ⑤Na.
| A. | ①②⑤ | B. | ①② | C. | ①②③ | D. | ①②③⑤ |
分析 游离态是元素以单质的形式存在,化合态是元素在化合物中的形式存在,元素在自然界中的存在状态与元素的活泼性有密切的关系,活泼元素在自然界中以化合物的形式存在,不活泼的元素在自然界中以单质的形式存在.
解答 解:①硅元素自然界中以硅酸盐或二氧化硅形式,不存在游离态的硅,故正确;
②Al为比较活泼的金属,易被氧化,从而性质活泼,在自然界中只能以化合物的形式存在,故正确;
③Cl最外层电子为7,易得到,易被还原,从而性质活泼,在自然界中只能以化合物的形式存在,故正确;
④Fe在自然界中以化合态,只有少量陨石中含有游离态铁,但陨石不算自然界,故错误;
⑤钠最外层电子少,易失去,易被氧化,从而性质活泼,在自然界中只能以化合物的形式存在,故正确;
故选D.
点评 本题考查了游离态、化合态的含义,元素在自然界中的存在状态与元素的活泼性有密切的关系,活泼元素在自然界中以化合物的形式存在,不活泼的元素在自然界中以单质的形式存在,题目较简单.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
19.下列属于物理变化的是( )
| A. | 石油的分馏 | B. | 淀粉水解 | C. | 蛋白质水解 | D. | 煤的干馏 |
6.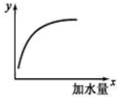 如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
 如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )| A. | c(H+)或 c(OH-) | B. | HA的电离平衡常数Ka | ||
| C. | c(H+)/c(HA) | D. | n(H+)或 n(OH-) |
3.25℃,101k Pa时,强酸与强碱的稀溶液发生中和反应生成1mol水时所放出的热量约为57.3kJ/mol;辛烷的燃烧热为5518kJ/mol.下列热化学方程式书写正确的是( )
| A. | CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.3kJ/mol | |
| B. | KOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$K2SO4(aq)+H2O(l)△H=-57.3kJ/mol | |
| C. | C8H18(l)+$\frac{25}{2}$ O2 (g)═8CO2 (g)+9H2O(g)△H=-5518 kJ/mol | |
| D. | 2C8H18(g)+25O2 (g)═16CO2 (g)+18H2O(1)△H=-5518 kJ/mol |
7.已知:还原性强弱:I->Fe2+.往100mL碘化亚铁溶液中缓慢通入3.36L(标准状况)氯气,反应完成后溶液中有$\frac{1}{2}$的Fe2+被氧化成Fe3+.则原碘化亚铁溶液的物质的量浓度为( )
| A. | 1.4mol•L-1 | B. | 1.2mol•L-1 | C. | 1.1mol•L-1 | D. | 1.0mol•L-1 |
8.下列实验所对应的离子方程式正确的是( )
| A. | 氢氧化铁与氢碘酸反应:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 向沸水中滴加饱和的氯化铁溶液:Fe3++3H2O═Fe(OH)3↓+3H+ | |
| C. | FeBr2溶液中通入足量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2++4Cl- | |
| D. | 向FeCl2溶液中加入少量K3[Fe(CN)6]溶液:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓ |

 ⑤
⑤ ⑥HOCH2CH2CH2COOH
⑥HOCH2CH2CH2COOH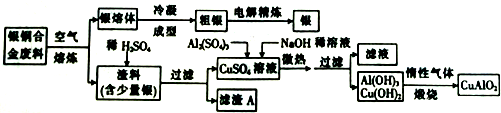
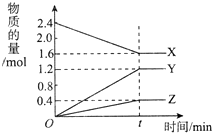 在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示.反应在t时刻达到平衡,据图回答下列问题:
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图所示.反应在t时刻达到平衡,据图回答下列问题: