题目内容
6.用锌块与20mL3mol•L-1硫酸反应制取H2,若要增大反应速率,可采取的措施是①再加入20mL同浓度的稀硫酸 ②加入几滴CuSO4溶液 ③改用粉末状锌 ④适当升高温( )| A. | ①②④ | B. | ②③④ | C. | ①③④⑤ | D. | ①②③④ |
分析 加快生成氢气的速率,可增大浓度,升高温度,增大固体的表面积以及形成原电池反应,以此解答.
解答 解:①再加入20mL同浓度的稀硫酸,浓度不变,反应速率不变,故错误;
②加入几滴CuSO4溶液,锌置换出铜,可形成原电池反应,加快反应速率,故正确;
③改用粉末状锌,固体表面积增大,反应速率增大,故正确;
④适当升高温,可增大反应速率,故正确.
故选B.
点评 本题考查化学反应速率的影响因素,侧重于基本概念的理解和应用,为高考常见题型和高频考点,难度不大,注意相关基础知识的积累.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
16.化学与社会、生活密切相关,下列说法正确的是( )
| A. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| B. | 工业上通常用电解Na、Mg、Al对应的氯化物制取该三种金属单质 | |
| C. | 石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化 | |
| D. | 燃料电池的燃料都在负极发生氧化反应 |
17.下列叙述正确的是( )
| A. | 甲苯、苯乙烯都既使酸性高锰酸钾褪色,也能使溴水褪色 | |
| B. | 塑料、橡胶和合成纤维都属于有机高分子化合物 | |
| C. | 肥皂是高级脂肪酸与甘油的酯化产物 | |
| D. | 石蜡是从石油中获取的油脂 |
14.已知H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ•mol-1,则反应HCl(g)═$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)的△H为( )
| A. | +184.6kJ•mol-1 | B. | -92.3kJ•mol-1 | C. | -69.2kJ•mol-1 | D. | +92.3kJ•mol-1 |
11.下列事实不能用勒夏特列原理解释的是( )
| A. | 氯水中有下列平衡Cl2+H2O═HCl+HClO,当加入硝酸银溶液后,溶液颜色变浅 | |
| B. | 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 | |
| C. | 氨水中加入NaOH固体有利于氨气的溢出 | |
| D. | pH=1的盐酸加水稀释到原体积的100倍后,PH=3 |
15.下列反应中,不属于化合、分解、置换、复分解等四种基本反应类型的是( )
| A. | CuSO4+H2S═CuS↓+H2SO4 | |
| B. | 2FeCl3+Cu═2FeCl2+CuCl2 | |
| C. | .Cu2 (OH)2CO3 $\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O | |
| D. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
9.已知锶(Sr)位于周期表第5周期第IIA族,则向饱和SrCO3溶液中加水,下列叙述正确的是( )
| A. | SrCO3的溶解度不变,KSP不变 | B. | SrCO3的溶解度不变,KSP增大 | ||
| C. | SrCO3的溶解度增大,KSP不变 | D. | SrCO3的溶解度减小,KSP增大 |
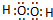 ,W第一步电离方程式为H2O2?H++HO2-.
,W第一步电离方程式为H2O2?H++HO2-.