题目内容
以下6种物质中选取序号填空(仅填序号,可重复选填).
①二氧化碳 ②硫化氢 ③氯化铵
④氢氧化钾 ⑤甲醛 ⑥乙醇
(1)含有非极性键的是 ;
(2)含有配位键的是 ;
(3)既含有σ键又含有π键的是 ;
(4)分子的立体结构呈平面三角形的是 ;
(5)属于非极性分子的是 ;
(6)属于离子化合物的是 .
①二氧化碳 ②硫化氢 ③氯化铵
④氢氧化钾 ⑤甲醛 ⑥乙醇
(1)含有非极性键的是
(2)含有配位键的是
(3)既含有σ键又含有π键的是
(4)分子的立体结构呈平面三角形的是
(5)属于非极性分子的是
(6)属于离子化合物的是
考点:共价键的形成及共价键的主要类型,判断简单分子或离子的构型,配合物的成键情况,极性分子和非极性分子
专题:化学键与晶体结构
分析:(1)同种非金属元素之间形成非极性共价键;
(2)形成配位键两个粒子,一方提供空轨道、一方提高孤对电子;
(3)既含有σ键又含有π键应为双键或三键;
(4)分子的立体结构呈平面三角形的为sp2杂化;
(5)结构对称,正负电荷重心重叠的分子为非极性分子;
(6)含有离子键的化合物为离子化合物.
(2)形成配位键两个粒子,一方提供空轨道、一方提高孤对电子;
(3)既含有σ键又含有π键应为双键或三键;
(4)分子的立体结构呈平面三角形的为sp2杂化;
(5)结构对称,正负电荷重心重叠的分子为非极性分子;
(6)含有离子键的化合物为离子化合物.
解答:
解:(1)乙醇中含有C-C键,为非极性键,故答案为:⑥;
(2)氯化铵中含有配位键,故答案为:③;
(3)二氧化碳和甲醛中分别含有C=C键、C=O键,含有σ键又含有π键,故答案为:①⑤;
(4)甲醛中C为sp2杂化,且无孤电子对,为平面三角形,故答案为:⑤;
(5)二氧化碳为直线形分子,结构对称,为非极性分子,故答案为:①;
(6)氯化铵、氢氧化钾含有离子键,为离子化合物,故答案为:③④.
(2)氯化铵中含有配位键,故答案为:③;
(3)二氧化碳和甲醛中分别含有C=C键、C=O键,含有σ键又含有π键,故答案为:①⑤;
(4)甲醛中C为sp2杂化,且无孤电子对,为平面三角形,故答案为:⑤;
(5)二氧化碳为直线形分子,结构对称,为非极性分子,故答案为:①;
(6)氯化铵、氢氧化钾含有离子键,为离子化合物,故答案为:③④.
点评:本题考查化学键及其分类,为高频考点,侧重于学生的分析能力的考查,明确元素的类别及元素的成键是解答本题的关键,难度较小.

练习册系列答案
相关题目
 2011年9月,中国女科学家屠呦呦获得被誉为诺贝尔奖“风向标”的拉斯克奖,这是中国医学界迄今为止获得的世界级最高级大奖.她获奖理由是:“因为创制新型抗疟药--青蒿素和双氢蒿素,挽救了全球特别是发展中国家的数百万人的生命.”已知结构如图所示,则下列说法正确的是( )
2011年9月,中国女科学家屠呦呦获得被誉为诺贝尔奖“风向标”的拉斯克奖,这是中国医学界迄今为止获得的世界级最高级大奖.她获奖理由是:“因为创制新型抗疟药--青蒿素和双氢蒿素,挽救了全球特别是发展中国家的数百万人的生命.”已知结构如图所示,则下列说法正确的是( )| A、青蒿素与维生素C一样易溶于水工作 |
| B、所有碳原子都可能在同一平面上 |
| C、青蒿素晶体为分子晶体,其化学式为C15H22O5,具有较强氧化性 |
| D、含有酯基,在胃酸作用下能水解,其水解产物能使氯化铁溶液显紫色 |
关于小苏打水溶液的表述正确的是( )
| A、c(Na+)=c(HCO3-)+2c(CO32-)+c(H2CO3) |
| B、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| C、c(Na+)>c(OH-)>c(HCO3-)>c(CO32-)>c(H+) |
| D、c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
 水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题:
水是一种重要的自然资源,是人类赖以生存不可缺少的物质.请回答下列问题: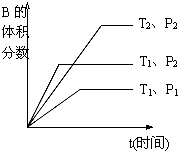 已知某可逆反应mA(g)+nB(g)?qC(g)+pD(s)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空(注:(2)、(3)、(4)题填“>”、“<”或“=”):
已知某可逆反应mA(g)+nB(g)?qC(g)+pD(s)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空(注:(2)、(3)、(4)题填“>”、“<”或“=”):