题目内容
下列叙述正确的是( )
| A、纯锌与硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 |
| B、甲醇和氧气以及KOH溶液构成的新型燃料电池中,其负极上发生的反应为:CH3OH+6OH-+6e-=CO2+5H2O |
| C、电解饱和食盐水制烧碱,NaOH在阳极区域产生 |
| D、用明矾净水是因为Al3+与OH-生成的Al(OH)3胶粒具有很强的吸附性 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.锌置换出铜,可形成原电池反应;
B.电解质溶液呈碱性,应生成碳酸钾;
C.电解饱和食盐水,阳极生成氯气,阴极生成氢气和氢氧化钠;
D.铝离子水解生成氢氧化铝胶体.
B.电解质溶液呈碱性,应生成碳酸钾;
C.电解饱和食盐水,阳极生成氯气,阴极生成氢气和氢氧化钠;
D.铝离子水解生成氢氧化铝胶体.
解答:
解:A.纯锌与硫酸反应时,加入少量CuSO4溶液,锌置换出铜,可形成原电池反应,加快反应速率,故A正确;
B.电解质溶液呈碱性,应生成碳酸钾,故B错误;
C.电解饱和食盐水,阳极生成氯气,阴极生成氢气和氢氧化钠,则NaOH在阴极区域产生,故C错误;
D.硫酸铝和水解生成氢氧化铝,因具有吸附性而达到净水的目的,故D错误.
故选A.
B.电解质溶液呈碱性,应生成碳酸钾,故B错误;
C.电解饱和食盐水,阳极生成氯气,阴极生成氢气和氢氧化钠,则NaOH在阴极区域产生,故C错误;
D.硫酸铝和水解生成氢氧化铝,因具有吸附性而达到净水的目的,故D错误.
故选A.
点评:本题考查较为综合,涉及原电池、电解池以及盐类的水解等知识,侧重化学与生活、生产的考查,注意相关知识的积累,难度不大.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
下列氯化物中,不能直接利用单质与氯气反应的得到是( )
| A、AlCl3 |
| B、NaCl |
| C、MgCl2 |
| D、FeCl2 |
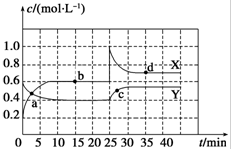 已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g);△H>0,现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g);△H>0,现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )| A、10min前反应向△H<0的方向进行 |
| B、曲线X表示N2O4浓度随时间的变化 |
| C、第二次达到平衡时,平衡常数的值大于0.9 |
| D、反应进行至25min时,曲线发生变化的原因是加入0.4molNO2 |
用惰性电极电解下列溶液一小段时间后,加入一定量的另一种物质(括号内),溶液能与原来溶液完全一样的是( )
| A、CuSO4[Cu(OH)2] |
| B、NaOH(NaOH) |
| C、NaCl(NaCl) |
| D、CuCl2(CuCl2) |
已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+;MnO4-→Mn2+;Cl2→2Cl-;KIO3→I2.如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
| A、Fe3+ |
| B、MnO4- |
| C、Cl2 |
| D、KIO3 |
下列反应属于放热反应的是( )
| A、浓硫酸溶于水 |
| B、氧化钙溶于水 |
| C、制水煤气的反应 |
| D、碳酸钙高温分解 |