题目内容
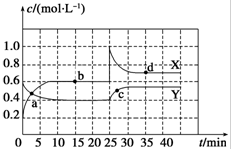 已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g);△H>0,现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g);△H>0,现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )| A、10min前反应向△H<0的方向进行 |
| B、曲线X表示N2O4浓度随时间的变化 |
| C、第二次达到平衡时,平衡常数的值大于0.9 |
| D、反应进行至25min时,曲线发生变化的原因是加入0.4molNO2 |
考点:物质的量或浓度随时间的变化曲线
专题:
分析:由图象曲线变化可知,在10min时,X浓度变化量为0.4mol/L,Y浓度变化量为0.2mol/L,则X为NO2的变化曲线,Y为N2O4的变化曲线,25min时,NO2的浓度增大,应为加入一定量的NO2,达到平衡的时间段为10min~25min以及30min以后,以此解答该题.
解答:
解:由图象曲线变化可知,在10min时,X浓度变化量为0.4mol/L,Y浓度变化量为0.2mol/L,则X为NO2的变化曲线,Y为N2O4的变化曲线,25min时,NO2的浓度增大,应为加入一定量的NO2,达到平衡的时间段为10min~25min以及30min以后,
A.由图象曲线变化可知,在10min前,NO2在增加,N2O4在减少,所以反应向正方向进行,即向△H>0的方向进行,故A错误;
B.根据上面的分析可知,X为NO2的变化曲线,故B错误;
C.根据图象可知,在第一次达到平衡时,平衡常数的值为
=0.9,第二次达到平衡时,由于温度不变,所以平衡常数的值不变,仍为0.9,故C错误;
D.25min时,NO2的浓度增大,应为加入0.4mol的NO2,故D正确.
故选D.
A.由图象曲线变化可知,在10min前,NO2在增加,N2O4在减少,所以反应向正方向进行,即向△H>0的方向进行,故A错误;
B.根据上面的分析可知,X为NO2的变化曲线,故B错误;
C.根据图象可知,在第一次达到平衡时,平衡常数的值为
| 0.62 |
| 0.4 |
D.25min时,NO2的浓度增大,应为加入0.4mol的NO2,故D正确.
故选D.
点评:本题考查化学平衡图象问题,题目难度中等,本题注意把握曲线的变化趋势,正确判断外界条件对平衡移动的影响

练习册系列答案
相关题目
下列四种烃的名称所表示的物质,命名正确的是( )
| A、2-甲基-2-丁炔 |
| B、1,4,5-三甲基苯 |
| C、3-甲基-2-丁烯 |
| D、2-甲基-2-丁烯 |
两份等质量的铝粉,一份投入足量的稀盐酸中,另一份投入足量的氢氧化钠溶液中,则生成氢气的质量比为( )
| A、2:3 | B、3:2 |
| C、36.5:40 | D、1:1 |
下列家庭垃圾中适合用于堆肥法处理的是( )
| A、废电池 | B、瓜果壳 |
| C、旧报纸 | D、塑料瓶 |
关于pH相同的醋酸和盐酸溶液,下列叙述中正确的是( )
| A、相同体积的酸中和氢氧化钠的量相同 |
| B、相同体积的酸分别稀释成相同PH溶液,所加水的量相同 |
| C、相同体积的酸与足量锌粒反应产生氢气的量相同 |
| D、两种酸溶液中阴离子总浓度相同 |
将3.48g Fe3O4(摩尔质量为232g/mol)完全溶解在足量硫酸溶液中,然后加入K2Cr2O7溶液25mL,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72-全部还原为Cr3+,则K2Cr2O7溶液的物质的量浓度为( )
| A、0.05 mol?L-1 |
| B、0.1 mol?L-1 |
| C、0.2mol?L-1 |
| D、0.3 mol?L-1 |
下列叙述正确的是( )
| A、纯锌与硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 |
| B、甲醇和氧气以及KOH溶液构成的新型燃料电池中,其负极上发生的反应为:CH3OH+6OH-+6e-=CO2+5H2O |
| C、电解饱和食盐水制烧碱,NaOH在阳极区域产生 |
| D、用明矾净水是因为Al3+与OH-生成的Al(OH)3胶粒具有很强的吸附性 |
下列说法正确的是( )
| A、铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
| B、铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| C、铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| D、镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
下列说法不正确的是( )
| A、Na2O2 晶体中阴离子和阳离子的数目之比为1:2 |
| B、同温同压下等质量的N2和CO两种气体的体积比为1:1 |
| C、同温同压下,相同体积的O2和O3两种气体中的氧原子个数比为1:1 |
| D、等质量的乙烯和环已烷所含质子数比为1:1 |