题目内容
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
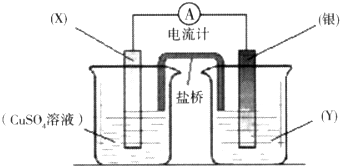
请回答:
(1)电极X的材料是 (填化学式,下同).
(2)在电解质溶液Y中所有离子的浓度大小关系是 .
(3)银电极为电池的 (填“正”或“负”)极,该极发生的电极反应是: .

请回答:
(1)电极X的材料是
(2)在电解质溶液Y中所有离子的浓度大小关系是
(3)银电极为电池的
考点:设计原电池
专题:电化学专题
分析:根据反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”分析,在反应中,Cu被氧化,失电子,应为原电池的负极,
电极反应为Cu-2e-=Cu2+,则正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,
电解质溶液为AgNO3 ,原电池中,电子从负极经外电路流向正极,以此解答该题.
电极反应为Cu-2e-=Cu2+,则正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,
电解质溶液为AgNO3 ,原电池中,电子从负极经外电路流向正极,以此解答该题.
解答:
解:(1)由反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”可知,在反应中,Cu被氧化,失电子,应为原电池的负极,Ag+在正极上得电子被还原,电解质溶液为AgNO3 ,
故答案为:Cu;
(2)电解质溶液为AgNO3 ,为强酸弱碱盐,水解呈酸性,离子浓度大小顺序为c(NO3-)>c(Ag+)>c(H+)>c(OH-),
故答案为:c(NO3-)>c(Ag+)>c(H+)>c(OH-);
(3)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,故答案为:正;Ag++e-=Ag.
故答案为:Cu;
(2)电解质溶液为AgNO3 ,为强酸弱碱盐,水解呈酸性,离子浓度大小顺序为c(NO3-)>c(Ag+)>c(H+)>c(OH-),
故答案为:c(NO3-)>c(Ag+)>c(H+)>c(OH-);
(3)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,故答案为:正;Ag++e-=Ag.
点评:本题考查原电池的设计及工作原理,注意电极反应式的书写方法,牢固掌握原电池中电极的判断,电极反应式的书写的方法性问题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各选项均有X、Y两种物质,将X缓缓滴入(通入)Y溶液中,无论X是否过量,均能用同一离子方程式表示的是( )
| X | Y | |
| A | 稀盐酸 | 碳酸钠溶液 |
| B | 偏铝酸钠溶液 | 硫酸溶液 |
| C | 氢氧化钠溶液 | 氯化铝溶液 |
| D | 二氧化碳 | 苯酚钠溶液 |
| A、A | B、B | C、C | D、D |
常温下往100mLFeCl3溶液中通入0.224L标况下的H2S,结果生成单质硫.再加入过量铁粉,反应停止后溶液中含有0.06mol阳离子.原FeCl3溶液的浓度是( )
| A、0.1mol/L |
| B、0.2mol/L |
| C、0.3mol/L |
| D、0.4mol/L |
下列电离方程式中,书写正确的是( )
| A、Ca(OH)2=Ca2++OH- |
| B、NaOH=Na++O2-+H+ |
| C、BaCl2=Ba2++Cl2- |
| D、K2SO4=2K++SO42- |
 实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示.
实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示. 2013年12月2日我国成功发射的“嫦娥三号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:SiO2+C+N2
2013年12月2日我国成功发射的“嫦娥三号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:SiO2+C+N2