题目内容
现有8种元素的性质、数据如下表所列,它们属于第二或第三周期.回答下列问题:
(1)③的元素符号是 ,⑧的元素名称是 .①在元素周期表中的位置是 (周期、族).
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 ;名称是 ;碱性最强的化合物的电子式是: ;属于 化合物(填“离子”或“共价”).
(3)比较④和⑦的氢化物的稳定性 (用化学式表示).
(4)用电子式表示①的氢化物的形成过程: .
(5)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式: .
(6)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式: .
| 编号号元素素性质质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)比较④和⑦的氢化物的稳定性
(4)用电子式表示①的氢化物的形成过程:
(5)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:
(6)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:第二、三周期元素中,元素①只有最低价-2,没有最高正化合价,则①为O;⑤有+7、-1价,则⑤为Cl;④⑦都有最高价+5,最低价-3,处于ⅤA族,原子半径④>⑦,故④为P、⑦为N;③⑥都有最高价+1,处于ⅠA族,原子半径③<⑥,则③为Li、⑥为Na;②有最高价+2,处于ⅡA族,原子半径大于Li,故②为Mg;⑧有最高价+3,处于ⅢA族,原子半径小于Cl,故⑧为B,据此解答.
解答:
解:第二、三周期元素中,元素①只有最低价-2,没有最高正化合价,则①为O;⑤有+7、-1价,则⑤为Cl;④⑦都有最高价+5,最低价-3,处于ⅤA族,原子半径④>⑦,故④为P、⑦为N;③⑥都有最高价+1,处于ⅠA族,原子半径③<⑥,则③为Li、⑥为Na;②有最高价+2,处于ⅡA族,原子半径大于Li,故②为Mg;⑧有最高价+3,处于ⅢA族,原子半径小于Cl,故⑧为B,
(1)由上述分析可知,③为Li,⑧为B,元素名称是硼,①为O,在元素周期表中的位置是:第二周期第ⅥA族,故答案为:Li;硼;第二周期第ⅥA族;
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,名称是高氯酸;碱性最强的化合物是NaOH,电子式是: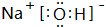 ,属于离子化合物,故答案为:HClO4,高氯酸;
,属于离子化合物,故答案为:HClO4,高氯酸;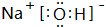 ,离子;
,离子;
(3)非金属性N>P,故氢化物稳定性:NH3>PH3,故答案为:NH3>PH3;
(4)①的氢化物为H2O,分子中H原子与O原子之间形成1对共用电子对,用H原子、O原子电子式表示其形成过程为: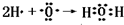 ,故答案为:
,故答案为: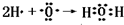 ;
;
(5)⑦的最高价氧化物对应水化物为硝酸,它的氢化物为氨气,二者反应生成硝酸铵,反应的化学方程式为:NH3+HNO3=NH4NO3,故答案为:NH3+HNO3=NH4NO3;
(6)②最高价氧化物对应水化物为Mg(OH)2,⑤的氢化物为HCl,氢氧化镁与盐酸反应生成氯化镁与水,反应的离子方程式为:Mg(OH)2+2H+=Mg2++2H2O,故答案为:Mg(OH)2+2H+=Mg2++2H2O.
(1)由上述分析可知,③为Li,⑧为B,元素名称是硼,①为O,在元素周期表中的位置是:第二周期第ⅥA族,故答案为:Li;硼;第二周期第ⅥA族;
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,名称是高氯酸;碱性最强的化合物是NaOH,电子式是:
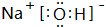 ,属于离子化合物,故答案为:HClO4,高氯酸;
,属于离子化合物,故答案为:HClO4,高氯酸;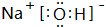 ,离子;
,离子;(3)非金属性N>P,故氢化物稳定性:NH3>PH3,故答案为:NH3>PH3;
(4)①的氢化物为H2O,分子中H原子与O原子之间形成1对共用电子对,用H原子、O原子电子式表示其形成过程为:
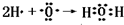 ,故答案为:
,故答案为: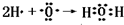 ;
;(5)⑦的最高价氧化物对应水化物为硝酸,它的氢化物为氨气,二者反应生成硝酸铵,反应的化学方程式为:NH3+HNO3=NH4NO3,故答案为:NH3+HNO3=NH4NO3;
(6)②最高价氧化物对应水化物为Mg(OH)2,⑤的氢化物为HCl,氢氧化镁与盐酸反应生成氯化镁与水,反应的离子方程式为:Mg(OH)2+2H+=Mg2++2H2O,故答案为:Mg(OH)2+2H+=Mg2++2H2O.
点评:本题考查结构性质位置关系应用,根据化合价与原子半径推断元素是解题关键,注意用电子式表示物质或化学键的形成,难度中等.

练习册系列答案
相关题目
Fe(OH)3胶体区别于FeCl3溶液的最本质特征是( )
| A、Fe(OH)3胶体能产生丁达尔现象 |
| B、Fe(OH)3胶体是均一的分散系 |
| C、Fe(OH)3胶体的分散质能透过滤纸 |
| D、Fe(OH)3胶体中分散质粒子的大小在1-100纳米之间 |
氯化铝溶液加热蒸干灼烧得到的固体主要成分是( )
| A、AlCl3 |
| B、Al(OH)3 |
| C、Al2O3 |
| D、Al |
 卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物.
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物.