题目内容
化学与科学、技术、社会、环境密切相关,下列有关说法正确的是( )
| A、锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去 |
| B、日本福岛核电站爆炸时释放的两种放射性核素13153I与13755Cs的中子数相等 |
| C、铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝 |
| D、海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化 |
考点:难溶电解质的溶解平衡及沉淀转化的本质,同位素及其应用,海水资源及其综合利用,合金的概念及其重要应用
专题:化学应用
分析:A、利用难溶电解质的溶解平衡及沉淀转化的本质;
B、中子数=质量数-质子数;
C、铝的冶炼用电解氧化铝的方法;
D、明矾只能作为净水剂,但不能使海水淡化.
B、中子数=质量数-质子数;
C、铝的冶炼用电解氧化铝的方法;
D、明矾只能作为净水剂,但不能使海水淡化.
解答:
解:A、硫酸钙的溶解度大于碳酸钙的溶解度,溶解度大的物质能向溶解度小的物质转化,所以锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去,故A正确;
B、131I的中子数=131-53=78,137Cs的中子数=137-55=82,故B错误;
C、一般来说,活泼金属用电解法;铝是活泼金属,所以采用电解法冶炼,故C错误;
D、明矾溶于水生成氢氧化铝胶体能吸附水中的悬浮颗粒,但不能除去海水中的盐分使海水淡化,故D错误,
故选A.
B、131I的中子数=131-53=78,137Cs的中子数=137-55=82,故B错误;
C、一般来说,活泼金属用电解法;铝是活泼金属,所以采用电解法冶炼,故C错误;
D、明矾溶于水生成氢氧化铝胶体能吸附水中的悬浮颗粒,但不能除去海水中的盐分使海水淡化,故D错误,
故选A.
点评:本题考查了沉淀的转化、胶体的性质、中子数的计算等知识点,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
向含有0.010mol?L-1 CrO42-离子和0.010mol?L-1 SO42-离子的混合溶液中,逐滴加入少量Pb(NO3)2溶液(忽略加入Pb(NO3)2所引起的体积变化),下列说法正确的是(KSP (PbCrO4)=2.8×10-13,KSP (PbSO4)=2.8×10-8)( )
| A、PbCrO4先沉淀 |
| B、PbSO4先沉淀 |
| C、PbCrO4和PbSO4一起沉淀 |
| D、PbCrO4和PbSO4都不沉淀 |
下列关于说法正确的是( )
| A、反应CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.1kJ?mol-1低温可自发进行 |
| B、常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4) |
| C、室温时,0.1mol/L某一元酸在水中有0.1%电离,此酸的电离平衡常数约为1×10-7 |
| D、将镁条和铝片用导线连接再插进稀NaOH溶液,镁条上产生气泡,说明铝比镁活泼 |
有关AgCl沉淀的溶解平衡,下列说法正确的是( )
| A、AgCl沉淀生成和沉淀溶解不断进行,但速率为0 |
| B、AgCl难溶于水,溶液中没有Ag+和Cl- |
| C、升高温度,AgCl沉淀的溶解度增大 |
| D、向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度不变 |
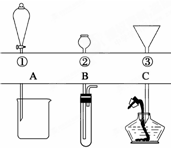 如图所示,①~③是几种漏斗的上部,A、B、C是实际操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图.请根据实际操作时上述漏斗的使用范围和它们的形状,指出A~C分别与①~③中哪一种最匹配(图中漏斗及容器中的药品和其他物品均已略去,铁架台、铁夹也已略去).A与
如图所示,①~③是几种漏斗的上部,A、B、C是实际操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图.请根据实际操作时上述漏斗的使用范围和它们的形状,指出A~C分别与①~③中哪一种最匹配(图中漏斗及容器中的药品和其他物品均已略去,铁架台、铁夹也已略去).A与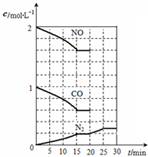 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.

