题目内容
2.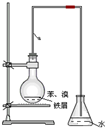 某同学设计如图装置制取少量溴苯,请回答下列问题:
某同学设计如图装置制取少量溴苯,请回答下列问题:①写出实验室制取溴苯的化学方程式
 .
.②上述反应发生后,在锥形瓶中加入硝酸银溶液观察到的现象是浅黄色沉淀,该装置中长直导管a的作用冷凝回流并导气,
③锥形瓶中的导管为什么不插入液面下?HBr极易溶于水,防止水倒吸入烧瓶中.
分析 制备溴苯,由实验装置可知,烧瓶内苯与液溴在催化剂作用下发生取代反应生成溴苯、HBr,长导管可冷凝回流,使溴、苯尽量充分反应,锥形瓶中HBr极易溶于水,导管在液面上可防止倒吸,溴离子与硝酸银反应生成淡黄色AgBr沉淀,以此来解答.
解答 解:①苯与液溴在催化剂条件下发生取代反应,即 ,故答案为:
,故答案为: ;
;
②上述反应发生后,在锥形瓶中加入硝酸银溶液观察到的现象是浅黄色沉淀,该装置中长直导管a的作用冷凝回流并导气,
故答案为:浅黄色沉淀;冷凝回流并导气;
③导管口不能插入锥形瓶中的液面之下,其原因是HBr极易溶于水,防止倒吸,故答案为:HBr极易溶于水,防止水倒吸入烧瓶中.
点评 本题考查有机物制备实验,为高频考点,把握制备实验原理、实验装置的作用、实验技能为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
1.下列物质属于醇类的是( )
| A. | 乙醇 | B. | 苯酚 | C. | 乙酸 | D. | 乙醛 |
2.下列关于苯的说法不正确的是( )
| A. | 分子式是C6H6 | |
| B. | 所有的原子在同一平面上 | |
| C. | 存在碳碳单键与碳碳双键交替出现的结构 | |
| D. | 能和浓硝酸浓硫酸的混合物在一定条件下发生取代反应 |
6.某离子反应中共有H20、H2C2O4、ClO3-、H+、CO2、ClO2六种微粒参与,已知在反应过程中溶液的pH逐渐增大.下列判断正确的是( )
| A. | 反应中CO2是还原产物 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 1mol H2C2O4参加反应转移4mol电子 | |
| D. | 当反应中有1mol电子转移时,有67.5g ClO2生成 |
7.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃,1.01×105Pa,64g SO2中含有的原子数为3NA | |
| B. | 足量Fe与1 mol Cl2反应,转移了3NA个电子 | |
| C. | 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 标准状况下,11.2L H2O含有的分子数为0.5NA |
14.反应3X(g)+Y(g)?Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.1mol,则此反应的平均速率v为( )
| A. | V(Y)=0.02mol•L-1•min-1 | B. | V(Z)=0.10mol•L-1•min-1 | ||
| C. | V(X)=0.03mol•L-1•min-1 | D. | V(W)=0.02mol•L-1•s-1 |
12.IUPAC宣布第113、115、117、118号元素存在,至此周期表中第七周期就完整了.下列说法错误的是( )
| A. | 118号是零族元素 | B. | 第七周期共有32种元素 | ||
| C. | 四种元素都有放射性 | D. | 四种元素都是金属 |

 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +HCl.
+HCl. .
. 制备高分子化合物
制备高分子化合物 的合成路线流程图(无机试剂任选),合成流程示意图如下:CH3CH2OH$→_{170℃}^{H_{2}SO_{4}}$CH2═CH2$→_{催化剂△}^{H_{2}}$CH3CH3.
的合成路线流程图(无机试剂任选),合成流程示意图如下:CH3CH2OH$→_{170℃}^{H_{2}SO_{4}}$CH2═CH2$→_{催化剂△}^{H_{2}}$CH3CH3.