题目内容
6.某离子反应中共有H20、H2C2O4、ClO3-、H+、CO2、ClO2六种微粒参与,已知在反应过程中溶液的pH逐渐增大.下列判断正确的是( )| A. | 反应中CO2是还原产物 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 1mol H2C2O4参加反应转移4mol电子 | |
| D. | 当反应中有1mol电子转移时,有67.5g ClO2生成 |
分析 ClO3-具有氧化性,H2C2O4具有还原性,二者发生氧化还原反应生成CO2、ClO2,在反应过程中溶液的pH逐渐增大,说明反应消耗H+,反应的离子方程式为2ClO3-+H2C2O4+2H+$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+2CO2↑+2H2O,反应中Cl元素化合价由+5价降低到+4价,C元素化合价由+3价升高到+4价,以此解答该题.
解答 解:ClO3-具有氧化性,H2C2O4具有还原性,二者发生氧化还原反应生成CO2、ClO2,在反应过程中溶液的pH逐渐增大,说明反应消耗H+,反应的离子方程式为2ClO3-+H2C2O4+2H+$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+2CO2↑+2H2O,
A.C元素化合价由+3价升高到+4价,CO2是氧化产物,故A错误;
B.由离子方程式可知氧化剂与还原剂物质的量之比为2:1,故B错误;
C.C元素化合价由+3价升高到+4价,则1mol H2C2O4参加反应转移2mol电子,故C错误;
D.反应中Cl元素化合价由+5价降低到+4价,当反应中有1mol电子转移时,生成1molClO2,质量为67.5g,故D正确.
故选D.
点评 本题以含氯化合物为载体考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念和转移电子数的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
相关题目
16.从海水提取溴的过程中,吸收塔内溴蒸气和吸收剂SO2发生的化学反应为:Br2+SO2+2H2O=2HBr+H2SO4,下列说法正确的是( )
| A. | SO2在反应中被还原 | B. | Br2在反应中失去电子 | ||
| C. | Br2在反应中表现氧化性 | D. | 1mol氧化剂在反应中得到1mol电子 |
17.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol氮气中所含的氮原子数是0.1NA | |
| B. | 标准状况下,2.24 L乙醇中所含的分子数是0.1NA | |
| C. | 1mol•L-1 氨水溶液中含NH4+的数目是NA | |
| D. | 24g镁和足量的盐酸反应,电子转移的数目是2NA |
14.可用于鉴别以下三种化合物的试剂组合是( )
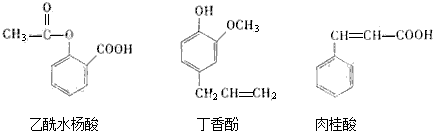
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④碳酸钠溶液.

①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液 ④碳酸钠溶液.
| A. | ②与③ | B. | ③与④ | C. | ①与④ | D. | ②与④ |
9.下列有关电解质溶液的说法正确的是( )
| A. | pH相同的 ①CH3COOK ②KHCO3 ③KClO三种溶液的c(K+):①>②>③ | |
| B. | 0.1mol/L NaHC2O4溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:C(Na+)>c(C2O42-)>c(HC2O4- )>c(OH-)>c(H+) | |
| C. | 常温下,0.1 mol/L Na2S溶液中存在:c(OH-)═c(H+)+c(HS-)+c(H2S) | |
| D. | 向0.2 mol•L-1的氨水中加入少量氯化铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 |
6.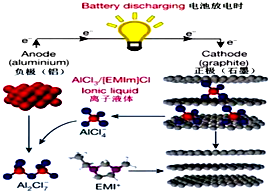 据2015年4月10日的报道,湖南大学 85后副教授鲁兵安参与斯坦福大学的团队刚刚发明出了一种“一分钟充满电”的新型铝离子电池.他们发现了一种新型石墨材料--泡沫石墨(graphite foam),泡沫石墨刚好可以充当电池的正极(负极用铝制成),而电解液则采用一种离子液体--即全由离子组成、室温下呈液态的离子化合物,具体成分为一种有机盐(化学表达式为[EMIm]Cl)与氯化铝的混合物.如图:关于该电池的说法不正确的是( )
据2015年4月10日的报道,湖南大学 85后副教授鲁兵安参与斯坦福大学的团队刚刚发明出了一种“一分钟充满电”的新型铝离子电池.他们发现了一种新型石墨材料--泡沫石墨(graphite foam),泡沫石墨刚好可以充当电池的正极(负极用铝制成),而电解液则采用一种离子液体--即全由离子组成、室温下呈液态的离子化合物,具体成分为一种有机盐(化学表达式为[EMIm]Cl)与氯化铝的混合物.如图:关于该电池的说法不正确的是( )
 据2015年4月10日的报道,湖南大学 85后副教授鲁兵安参与斯坦福大学的团队刚刚发明出了一种“一分钟充满电”的新型铝离子电池.他们发现了一种新型石墨材料--泡沫石墨(graphite foam),泡沫石墨刚好可以充当电池的正极(负极用铝制成),而电解液则采用一种离子液体--即全由离子组成、室温下呈液态的离子化合物,具体成分为一种有机盐(化学表达式为[EMIm]Cl)与氯化铝的混合物.如图:关于该电池的说法不正确的是( )
据2015年4月10日的报道,湖南大学 85后副教授鲁兵安参与斯坦福大学的团队刚刚发明出了一种“一分钟充满电”的新型铝离子电池.他们发现了一种新型石墨材料--泡沫石墨(graphite foam),泡沫石墨刚好可以充当电池的正极(负极用铝制成),而电解液则采用一种离子液体--即全由离子组成、室温下呈液态的离子化合物,具体成分为一种有机盐(化学表达式为[EMIm]Cl)与氯化铝的混合物.如图:关于该电池的说法不正确的是( )| A. | 放电时,铝电极的电极反应式为:Al+7AlCl4--3e-═4Al2Cl7- | |
| B. | [EMIm]Cl中既含离子键,又含共价键 | |
| C. | 电子流向为:石墨通过离子液体流向铝 | |
| D. | 充电时石墨电极的电极反应式为:Cn[AlCl4]-e-═Cn+AlCl4- |
7.塑化剂(DCHP)常用于塑料加工,其中一种制备方法如下:
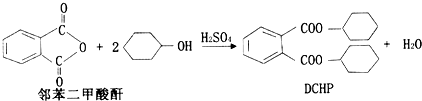
下列说法正确的是( )

下列说法正确的是( )
| A. | DCHP的分子式为C20H28O4 | |
| B. | 上述制备DCHP的反应属于取代反应 | |
| C. | DCHP苯环上的一氯代物有4种 | |
| D. | 1molDCHP最多可与含4molNaOH的溶液反应 |
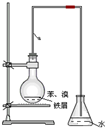 某同学设计如图装置制取少量溴苯,请回答下列问题:
某同学设计如图装置制取少量溴苯,请回答下列问题: .
.