题目内容
18.过氧乙酸是一种弱酸性氧化剂,极不稳定,广泛用作漂白剂和高效杀菌消毒剂等.Ⅰ、制备:冰醋酸与H2O2浓溶液按体积比1:1混合,加入适量浓硫酸,控制温度5℃~30℃,搅拌30min并静置4~6h.反应原理为:H2O2+CH3COOH$\stackrel{浓H_{2}SO_{4}}{→}$
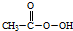 (过氧乙酸)+H2O
(过氧乙酸)+H2OⅡ、含量测定:称取5.0000g过氧乙酸试样(液体),稀释至100mL备用.取上述稀释后过氧乙酸试样5.00mL,用0.0100mol•L-1KMnO4溶液滴定到终点以除去其中的H2O2,随即加入10%KI溶液10mL(足量),加入0.5%淀粉溶液3滴,摇匀,并用0.0500mol•L-1Na2S2O3标准溶液滴定到终点离子反应方程式为:I2+2S2O32-=2I-+S4O62-),消耗Na2S2O3标准溶液的总体积为20.00mL.
(1)制备过氧乙酸时,温度不宜过高,其原因可能是温度过高H2O2和CH3COOOH会分解.
(2)稀释样品时,除用到烧杯及玻璃棒外,还用到的玻璃仪器有100mL容量瓶、胶头滴管.
(3)用Na2S2O3标准溶液滴定到终点的现象是溶液蓝色刚好褪去,且半分钟不变化.
(4)通过计算确定原试样中过氧乙酸的质量分数(写出计算过程).
分析 (1)温度过高时过氧化氢会分解不能保证其和醋酸充分反应,同时过氧乙酸也容易分解;
(2)称取5.0000g过氧乙酸试样(液体),稀释至100mL时,除用到烧杯及玻璃棒外,还要用到胶头滴管取液体,要用100mL容量瓶定容;
(3)用Na2S2O3标准溶液滴定到终点时,溶液中的碘全部参加反应,溶液的蓝色会褪色,据此答题;
(4)根据(3)的方程式及I2+2S2O32-=2I-+S4O62-两个化学方程式,可以得关系式如下:CH3COOOH~I2~2Na2S2O3,据此计算稀释后5mL反应中n(CH3COOOH),进而计算原试样中过氧乙酸的质量分数.
解答 解:(1)温度过高时过氧化氢会分解不能保证其和醋酸充分反应,同时过氧乙酸也容易分解,
故答案为:温度过高H2O2和CH3COOOH会分解;
(2)称取5.0000g过氧乙酸试样(液体),稀释至100mL时,除用到烧杯及玻璃棒外,还要用到胶头滴管取液体,要用100mL容量瓶定容,
故答案为:100mL容量瓶;胶头滴管;
(3)用Na2S2O3标准溶液滴定到终点时,溶液中的碘全部参加反应,溶液的蓝色会褪色,所以滴定到终点的现象是溶液蓝色刚好褪去,且半分钟不变化,
故答案为:溶液蓝色刚好褪去,且半分钟不变化;
(4)根据(3)的方程式及I2+2S2O32-=2I-+S4O62-两个化学方程式,可以得关系式如下:CH3COOOH~I2~2Na2S2O3,由关系式可知,n(CH3COOOH)=$\frac{1}{2}$n(Na2S2O3)=$\frac{1}{2}$×0.05mol/L×0.02L=5×10-4mol,故原样品中w(CH3COOOH)=$\frac{5×1{0}^{-4}mol×76g/mol}{5g×\frac{5ml}{100ml}}$×100%=15.2%,
答:原试样中过氧乙酸的质量分数为15.2%.
点评 本题考查氧化还原反应滴定、实验原理的分析和多步反应关系的计算等,难度中等,(4)中注意利用关系式进行计算,为易错点,学生容易忽略滴定中所取溶液的体积,按稀释后溶液体积计算,导致错误答案.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 用稀硫酸清洗铁锈(Fe2O3):Fe2O3+6H+═2Fe3++3H2O | |
| B. | 铝片与硝酸汞溶液反应:Al+Hg2+═Al3++Hg | |
| C. | 硫酸铜溶液和氢氧化钡溶液混合:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ |
| A. | 标准状况下,同体积的气体A和气体B的质量比m:n | |
| B. | 25℃,101KPa时,1Kg气体A与1Kg气体B的分子数比为n:m | |
| C. | 同温同压下,气体A与气体B密度比为n:m | |
| D. | 标准状况下,等质量的A与B的体积比为n:m |
| A. | 滴定前,滴定管尖嘴部分有气泡,滴定后气泡消失 | |
| B. | 锥形瓶沾有少量水 | |
| C. | 以甲基橙作指示剂 | |
| D. | 滴定前仰视滴定管读数,滴定后平视刻度读数 |
Ⅰ.配制0.50mol•L-1NaOH溶液
(1)若实验中大约要使用470mL NaOH溶液,至少需要称量NaOH固体10.0 g.
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):a、b、e.
| 名称 | 托盘天平 | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 | 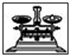 |  |  | 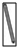 |  | |
| 序号 | a | b | c | d | e | f |
(2)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如下表.①请填写下表中的空白:
| 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
③上述实验数值结果与57.3kJ•mol-1有偏差,产生偏差的原因可能是(填字母)A、C、D.
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
| A. | 在有AgCl沉淀的溶液中加入NaC1固体,c(Ag+)减小 | |
| B. | 室温下100mL pH=1.3的Ba(OH)2溶液中OH-的物质的量为0.02 mol | |
| C. | 稀释0.1 mol/L的NH3•H2O溶液,溶液中所有离子浓度均减小 | |
| D. | 溶液中水电离出c(H+)和水电离出的c(OH-)的乘积一定等于10-14 |
 某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:
某化学实验小组用0.2000 mol/L的酸性KMnO4溶液测定草酸晶体的纯度(草酸晶体化学式为H2C2O4•2H2O,杂质不与KMnO4反应).实验步骤如下:(1)称取13.0 g草酸晶体,配成250.00 mL水溶液.此操作过程所需用到的仪器是:天平(含砝码)、烧杯、药匙、玻璃棒、胶头滴管和250 mL容量瓶
(2)量取草酸溶液25.00 mL放入锥形瓶中,用0.2000 mol/L的酸性KMnO4溶液滴定.
①量取25.00 mL草酸溶液的仪器是25mL酸式滴定管(或25mL移液管).
②滴定时,KMnO4溶液应装在酸式 (填“酸式”、“碱式”)滴定管中.
③滴定时所发生反应的离子方程式:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O.
④滴定达到终点的标志是加入最后一滴高锰酸钾溶液,锥形瓶内溶液由无色变为红色,且半分钟不褪色.
(3)按正确操作测得有关数据记录如下:
| 滴定次数 | 草酸溶液体积 | 酸性KMnO4溶液体积 | |
| 滴定前读数/m L | 滴定后读数/m L | ||
| 第一次 | 25.00 | 0.20 | 20.58 |
| 第二次 | 25.00 | 4.00 | 24.40 |
| 第三次 | 25.00 | 2.38 | a |
②草酸晶体的纯度为98.86%(结果保留两位小数).
(4)在上述实验中,下列操作(其它操作正确)一定会造成测定结果偏高的是BD.
A.称取13.0 g草酸晶体时,将草酸晶体放在托盘天平右盘
B.锥形瓶水洗后用草酸溶液润洗
C.读取KMnO4溶液体积时,开始仰视读数,滴定结束时俯视读数
D.盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失.
 学生用0.1000mol•L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分为:
学生用0.1000mol•L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分为: