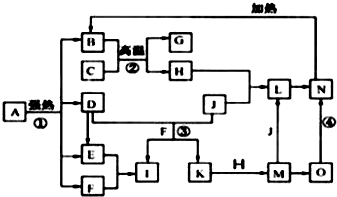
题目内容
实验室需要配制1mol?L-1的硫酸2L,需取用18.4mol?L-1的浓硫酸(密度为1.84g?mL-1)多少这毫升?(保留一位小数)
考点:溶液的配制
专题:计算题
分析:根据溶液稀释前后物质的量不变计算所需浓硫酸的体积.
解答:
解:稀释前后溶质的物质的量不变,设浓硫酸的体积为Vml,则1mol?L-1×2000ml=V×18.4mol?L-1,解得V≈108.7,所以需要浓硫酸的体积为108.7ml,
答:需取用18.4mol?L-1的浓硫酸108.7ml.
答:需取用18.4mol?L-1的浓硫酸108.7ml.
点评:本题考查了物质的量浓度的相关计算,题目难度不大,抓住稀释前后溶质的物质的量不变是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
分析:在4Fe3++2H2O=4Fe2++4H++O2↑反应中,每生成标准状况下22.4LO2,电子转移的个数为( )
| A、6.02×1023 |
| B、1.806×1024 |
| C、1.204×1024 |
| D、2.408×1024 |
从柑桔中炼制萜二烯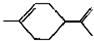 ,下列有关它的推测不正确的是( )
,下列有关它的推测不正确的是( )
 ,下列有关它的推测不正确的是( )
,下列有关它的推测不正确的是( )| A、分子式为C10H16 |
| B、常温下为液态,难溶于水 |
C、与过量的溴的CCl4溶液反应后产物为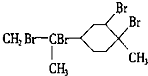 |
| D、它不能使酸性高锰酸钾溶液褪色 |
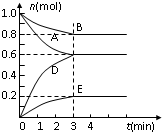 T℃、2L密闭容器中某一反应不同时刻各物质的量如图(E为固体,其余为气体).回答下列问题:
T℃、2L密闭容器中某一反应不同时刻各物质的量如图(E为固体,其余为气体).回答下列问题: