题目内容
9.设NA表示阿伏加德罗常数的值,下列说法错误的是( )| A. | 常温常压下,32gO2和O3的混合气体所含质子数一定为16NA | |
| B. | 标准状况下,11.2LSO2中含有的分子数为0.5NA | |
| C. | 常温下,5.6 g铁与硝酸反应,失去的电子数一定为0.3 NA | |
| D. | 39g钾与足量氧气充分反应,转移的电子数一定是NA |
分析 A.依据氧元素守恒计算氧原子数及氧原子所含质子数解答;
B.依据n=$\frac{V}{Vm}$计算二氧化硫的物质的量;
C.铁的化合价由+2和+3价,5.6g铁的物质的量为0.1mol,0.1mol铁与稀硝酸反应,如果生成亚铁离子,失去的电子为0.2mol;
D.39g钾与足量氧气充分反应,生成物质中钾化合价都是+1价.
解答 解:A.1个氧原子含有8个质子,常温常压下32gO2与O3混合气中含有氧原子数目=$\frac{32g}{16g/mol}$×NA=2NA,含有质子数为2NA×8=16NA,故A正确;
B.标准状况下,11.2LSO2中含有的分子物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,含有分子数为0.5NA,故B正确;
C.5.6g铁的物质的量为0.1mol,如果生成亚铁离子,反应失去0.2mol电子,如果生成铁离子,失去的电子为0.3mol,所以失去的电子数不一定为0.3NA,故C错误;
D.39g钾物质的量为1mol,与足量氧气充分反应,生成1mol+1价钾离子,转移的电子数一定是NA,故D正确;
故选:C.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件是解题关键,注意铁与硝酸反应产物与硝酸用量有关,题目难度中等.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
19.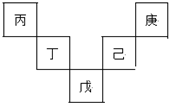 已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
 已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )| A. | 丙与戊的原子序数相差28 | |
| B. | 常温下,庚的单质能与水反应产生气体 | |
| C. | 气态氢化物的稳定性:庚<己<戊 | |
| D. | 丁的最高价氧化物可用于制造光导纤维 |
20.中药狼把草的成分之一M具有清炎杀菌作用,M的结构如图所示下列叙述正确的是( )

| A. | M的摩尔质量是178 | |
| B. | 1 mol M最多能与2mol Br2发生反应 | |
| C. | 1mol M与足量NaHCO3反应能生成2 mol CO2 | |
| D. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 |
17.如图所示,a、b都是惰性电极,通电一段时间后,a极附近溶液显红色.下列说法中正确的是( )
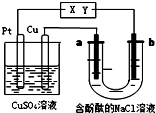

| A. | CuSO4溶液的n(SO42-)保持不变 | B. | U型管中溶液pH值逐渐变小 | ||
| C. | CuSO4溶液的c(Cu2+)逐渐减小 | D. | X是正极,Y是负极 |
4.某卤代烷烃C5H11Cl发生消去反应时,可以得到两种烯烃,则该卤代烷烃的结构简式可能为( )
| A. | CH3CH2CH2CH2Cl | B. | CH3CH2-CHCl-CH2CH3 | ||
| C. | CH3-CHCl-CH2CH2CH3 | D. | (CH3)3CCH2Cl |
18.美国劳仑斯国家实验室曾在1999年宣布用86Kr离子轰击208Pb靶得到118号元素的一种原子,其质量数为293.其后,反复实验均未能重现118号元素的信号,因此该实验室在2001年8月宣布收回该论文.但是科学家们相信,完成的第七周期包含的元素数目与第六周期相同.若118号元素将来被确认,则下列预测不合理的是 ( )
| A. | 它的中子数是175 | B. | 它是第七周期元素 | ||
| C. | 它是活泼的金属元素 | D. | 它的最外层电子数是8 |
19.铝热反应可用于焊接钢轨,其反应方程式为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,该反应为( )
| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
