题目内容
19.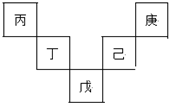 已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )| A. | 丙与戊的原子序数相差28 | |
| B. | 常温下,庚的单质能与水反应产生气体 | |
| C. | 气态氢化物的稳定性:庚<己<戊 | |
| D. | 丁的最高价氧化物可用于制造光导纤维 |
分析 己的最高价氧化物对应水化物有强脱水性,则为浓硫酸,可知己为S元素,丁原子最外层电子数是最内层电子数的2倍,结合位置关系可知丁为Si,丙为B,庚为F,戊为As,然后结合元素周期律及元素化合物知识来解答.
解答 解:己的最高价氧化物对应水化物有强脱水性,则为浓硫酸,可知己为S元素,丁原子最外层电子数是最内层电子数的2倍,结合位置关系可知丁为Si,丙为B,庚为F,戊为As,
A.丙与戊的原子序数相差为33-5=28,故A正确;
B.常温下,庚的单质F2与水反应生成氧气,故C正确;
C.非金属性越强,气态氢化物越稳定,则气态氢化物的稳定性:庚>己>戊,故C错误;
D.丁为Si,丁的最高价氧化物为SiO2,可用于制造光导纤维,故D正确;
故选C.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、原子结构推断元素等为解答的关键,侧重分析与应用能力的考查,注意元素周期律的应用,题目难度不大.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
9.下列有关实验操作能达到相应目的是( )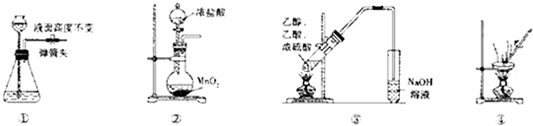

| A. | 装置①所示气密性良好 | |
| B. | 装置②可用于实脸室制取氯气 | |
| C. | 装置③可用于制取并收集乙酸乙脂 | |
| D. | 装置④可用于除去硫酸铜晶体中的结晶水 |
7.下列指定反应的离子方程式正确的是( )
| A. | 向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2++2H+=Ag++2NH4+ | |
| B. | 向Na2O2中加入足量的水:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| C. | 向硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ | |
| D. | 向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
4.下列关于铍元素及其化合物的性质的推测正确的是( )
| A. | 铍原子的半径大于硼原子的半径 | |
| B. | 相同条件下,单质铍与酸反应比与单质锂与酸反应剧烈 | |
| C. | 氢氧化铍的碱性比氢氧化钙的碱性强 | |
| D. | 单质铍能与冷水剧烈反应 |
11.某有机物的结构简式如下,关于该有机物的下列叙述不正确的是( )


| A. | 不能发生消去反应 | |
| B. | 能使溴水褪色 | |
| C. | 在加热和催化剂作用下,最多能与4 mol H2反应 | |
| D. | 一定条件下,能发生取代反应 |
9.设NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A. | 常温常压下,32gO2和O3的混合气体所含质子数一定为16NA | |
| B. | 标准状况下,11.2LSO2中含有的分子数为0.5NA | |
| C. | 常温下,5.6 g铁与硝酸反应,失去的电子数一定为0.3 NA | |
| D. | 39g钾与足量氧气充分反应,转移的电子数一定是NA |
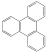 的一氯取代物有2种
的一氯取代物有2种 某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)?2C(g)达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示.
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)?2C(g)达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示.