题目内容
某研究性学习小组为探究草酸亚铁晶体的化学性质,进行了下列实验.已知草酸亚铁晶体(FeC2O4?2H2O)呈浅黄色,其中C元素的化合价为+3价.
(1)向盛有草酸亚铁晶体的试管中滴入几滴H2SO4酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到有CO2气体生成.这说明草酸亚铁晶体具有 (填“氧化性”、“还原性”或“碱性”).若此反应中消耗2molFeC2O4?2H2O,则参加反应的KMnO4为 mol.
(2)查阅资料表明:草酸亚铁晶体在密闭容器中加热到一定温度时完全分解,生成几种氧化物,残留物为黑色固体.请你根据课本上介绍的铁的氧化物的物理性质,对黑色固体的组成提出如下假设,完成假设二和假设三:
假设一:全部是FeO 假设二 :假设三 :
(3)为验证上述假设一是否成立,课题组进行如下研究.
【定性研究】请你完成下表中内容.
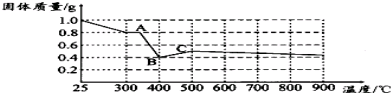
【定量研究】资料表明FeC2O4?2H2O受热分解时,固体质量随温度变化的曲线如下图所示.请你写出加热到400℃时,FeC2O4?2H2O晶体受热分解(生成几种氧化物)的化学方程式为:
(1)向盛有草酸亚铁晶体的试管中滴入几滴H2SO4酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到有CO2气体生成.这说明草酸亚铁晶体具有
(2)查阅资料表明:草酸亚铁晶体在密闭容器中加热到一定温度时完全分解,生成几种氧化物,残留物为黑色固体.请你根据课本上介绍的铁的氧化物的物理性质,对黑色固体的组成提出如下假设,完成假设二和假设三:
假设一:全部是FeO 假设二
(3)为验证上述假设一是否成立,课题组进行如下研究.
【定性研究】请你完成下表中内容.
| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| 取少量黑色固体, |

考点:性质实验方案的设计
专题:实验设计题
分析:(1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成.说明草酸亚铁被氧化为铁离子、二氧化碳气体,草酸亚铁具有还原性,依据电子守恒计算得到消耗的高锰酸钾物质的量;
(2)草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体可能为氧化亚铁或四氧化三铁,分析判断;
(3)氧化亚铁溶解于盐酸生成氯化亚铁溶液,加入KSCN溶液,若溶液不变红证明假设一正确;
定量实验:根据图中提供的信息,通过计算可以判断反应的化学方程式和物质的化学式.
(2)草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体可能为氧化亚铁或四氧化三铁,分析判断;
(3)氧化亚铁溶解于盐酸生成氯化亚铁溶液,加入KSCN溶液,若溶液不变红证明假设一正确;
定量实验:根据图中提供的信息,通过计算可以判断反应的化学方程式和物质的化学式.
解答:
解:(1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成.说明草酸亚铁被氧化为铁离子、二氧化碳气体,草酸亚铁具有还原性,依据电子守恒计算得到消耗的高锰酸钾物质的量,依据氧化还原反应电子守恒原子守恒配平书写离子方程式为:
5Fe2++5C2O42-+3MnO4-+24H+=5Fe3++3Mn2++5CO2↑+12H2O,消耗2mol FeC2O4?2H2O,则参加反应的KMnO4为1.2mol;
故答案为:还原性;1.2;
(2)假设一:全部是氧化亚铁;假设二:全部是四氧化三铁;假设三:氧化亚铁和四氧化三铁的混合物,
故答案为:全部是四氧化三铁;氧化亚铁和四氧化三铁的混合物;
(3)[定性研究]实验步聚:取少量黑色固体,加入适量的稀盐酸(或稀硫酸)溶解,在溶液中加入KSCN溶液.现象与结论:若溶液不变红,则假设一成立,若溶液变红,则假设一不成立;
故答案为:取少量黑色固体,加入适量的稀盐酸(或稀硫酸)溶解,在溶液中加入KSCN溶液,若溶液不变红,则假设一成立,若溶液变红,则假设一不成立;
[定量研究]通过剩余固体的质量可知,过程Ⅰ发生的反应是:草酸亚铁晶体受热失去结晶水,设失去结晶水x,图象分析可知固体质量变化1.0-0.8=0.2g,依据则反应的化学方程式计算为:
FeC2O4?2H2O
FeC2O4?(2-x)H2O+xH2O△m
180 18x
1.0 0.2
x=2
加热到300°C,晶体全部失去结晶水生成草酸亚铁和水,
继续加热到400°C,固体质量减少0.8g-0.4g=0.4g;此时草酸亚铁分解减少的是气体质量,反应过程中一定存在反应生成氧化亚铁和二氧化碳,铁元素化合价不变时,依据元素化合价变化和电子守恒可知碳元素化合价从+3价变化为+4价,一定有化合价降低生成+2价的一氧化碳,反应的化学方程式FeC2O4
FeO+CO+CO2,
FeC2O4
FeO+CO+CO2 △m
144 72
0.8 0.4
计算结果符合图象固体质量变化,所以反应的化学方程式为FeC2O4
FeO+CO+CO2 ,
故答案为:FeC2O4
FeO+CO+CO2 .
5Fe2++5C2O42-+3MnO4-+24H+=5Fe3++3Mn2++5CO2↑+12H2O,消耗2mol FeC2O4?2H2O,则参加反应的KMnO4为1.2mol;
故答案为:还原性;1.2;
(2)假设一:全部是氧化亚铁;假设二:全部是四氧化三铁;假设三:氧化亚铁和四氧化三铁的混合物,
故答案为:全部是四氧化三铁;氧化亚铁和四氧化三铁的混合物;
(3)[定性研究]实验步聚:取少量黑色固体,加入适量的稀盐酸(或稀硫酸)溶解,在溶液中加入KSCN溶液.现象与结论:若溶液不变红,则假设一成立,若溶液变红,则假设一不成立;
故答案为:取少量黑色固体,加入适量的稀盐酸(或稀硫酸)溶解,在溶液中加入KSCN溶液,若溶液不变红,则假设一成立,若溶液变红,则假设一不成立;
[定量研究]通过剩余固体的质量可知,过程Ⅰ发生的反应是:草酸亚铁晶体受热失去结晶水,设失去结晶水x,图象分析可知固体质量变化1.0-0.8=0.2g,依据则反应的化学方程式计算为:
FeC2O4?2H2O
| ||
180 18x
1.0 0.2
x=2
加热到300°C,晶体全部失去结晶水生成草酸亚铁和水,
继续加热到400°C,固体质量减少0.8g-0.4g=0.4g;此时草酸亚铁分解减少的是气体质量,反应过程中一定存在反应生成氧化亚铁和二氧化碳,铁元素化合价不变时,依据元素化合价变化和电子守恒可知碳元素化合价从+3价变化为+4价,一定有化合价降低生成+2价的一氧化碳,反应的化学方程式FeC2O4
| ||
FeC2O4
| ||
144 72
0.8 0.4
计算结果符合图象固体质量变化,所以反应的化学方程式为FeC2O4
| ||
故答案为:FeC2O4
| ||
点评:本题考查了铁及其化合物性质的实验验证和实验分析判断,定量计算,图象分析是解题关键,题目难度较大.

练习册系列答案
相关题目
实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格是( )
| A、1000mL |
| B、950mL |
| C、900mL |
| D、500mL |
在常温下,下列有关溶液中微粒的物质的量浓度关系不正确的是( )
| A、0.1 mol?L-1 Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| B、0.1 mol?L-1 pH=8的NH4HCO3溶液中:c(HCO3-)>c(NH4+)>c(OH-)>c(H+) |
| C、浓度均为0.1 mol?L-1的NH3?H2O溶液和NH4Cl溶液等体积混合:c(NH4+)+c(H+)>c(NH3?H2O)+c(OH-) |
| D、0.1 mol?L-1 Na2S溶液与0.1 mol?L-1 NaHS溶液等体积混合:2c(Na+)-3c(S2-)=3c(HS-)+3c(H2S) |
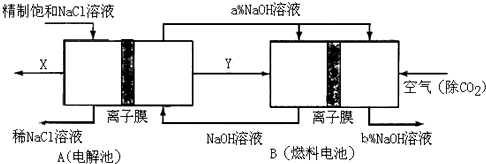
 乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表: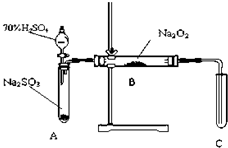 化学兴趣小组同学运用类比学习的思想,探究过氧化钠与二氧化硫的反应.小组同学改进了如图所示的装置进行实验制取SO2的反应.充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.试回答下列问题:
化学兴趣小组同学运用类比学习的思想,探究过氧化钠与二氧化硫的反应.小组同学改进了如图所示的装置进行实验制取SO2的反应.充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.试回答下列问题: