题目内容
工业上用电解饱和NaCl溶液的方法来制取NaOH、H2和Cl2,并以它们为原料生产一系列化工产品,称为氯碱工业.
(1)氯碱厂的盐酸车间可用氯气、氢气为原料进行生产,试写出其化合的化学方程式 .
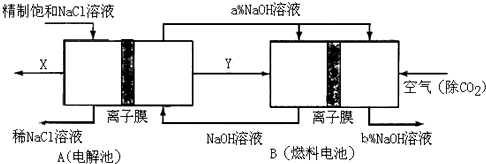
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,其相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.
①图中X、Y分别是 、 ,分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
②分别写出燃料电池B中的电极反应,正极: ; 负极: .

(1)氯碱厂的盐酸车间可用氯气、氢气为原料进行生产,试写出其化合的化学方程式
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,其相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过.
①图中X、Y分别是
②分别写出燃料电池B中的电极反应,正极:
考点:氯碱工业
专题:
分析:(1)根据氢气和氯气在点燃的条件下发生生成氯化氢来书写;
(2)在燃料电池中,通入空气的极是正极,氧气发生得电子的还原反应,通入燃料的极是负极,发生氧化反应,结合电解质溶液是氢氧化钠溶液,即可写出电极反应式,氢氧燃料电池最后产生的是水,能将电解质稀释,据此回答判断.
(2)在燃料电池中,通入空气的极是正极,氧气发生得电子的还原反应,通入燃料的极是负极,发生氧化反应,结合电解质溶液是氢氧化钠溶液,即可写出电极反应式,氢氧燃料电池最后产生的是水,能将电解质稀释,据此回答判断.
解答:
解:(1)氢气和氯气在点燃的条件下发生生成氯化氢,化学方程式为:H2+Cl2
2HCl,故答案为:H2+Cl2
2HCl;
(2)①由于在燃料电池中氧气在正极放电,可燃性气体在负极放电,所以通入空气的极是正极,则通入可燃性气体Y的极是负极,根据在氯碱工业中,电解食盐水除了生成NaOH还生成氯气和氢气,和空气形成燃料电池的为氢气,即Y是氢气,则X是氯气,氢氧燃料电池最后产生的是水,所以a%小于b%,故答案为:Cl2;H2;b%>a%;
②在燃料电池中,氧气在正极放电,由于电解质溶液为氢氧化钠溶液,故正极的电极反应式为:O2+4e-+2H2O=4OH-;
氢气在负极失电子,由于电解质溶液为氢氧化钠溶液,故负极的电极反应式为:2H2+4OH--4e-=4H2O,
故答案为:O2+4e-+2H2O=4OH-;2H2+4OH--4e-=4H2O.
| ||
| ||
(2)①由于在燃料电池中氧气在正极放电,可燃性气体在负极放电,所以通入空气的极是正极,则通入可燃性气体Y的极是负极,根据在氯碱工业中,电解食盐水除了生成NaOH还生成氯气和氢气,和空气形成燃料电池的为氢气,即Y是氢气,则X是氯气,氢氧燃料电池最后产生的是水,所以a%小于b%,故答案为:Cl2;H2;b%>a%;
②在燃料电池中,氧气在正极放电,由于电解质溶液为氢氧化钠溶液,故正极的电极反应式为:O2+4e-+2H2O=4OH-;
氢气在负极失电子,由于电解质溶液为氢氧化钠溶液,故负极的电极反应式为:2H2+4OH--4e-=4H2O,
故答案为:O2+4e-+2H2O=4OH-;2H2+4OH--4e-=4H2O.
点评:本题考查学生电解池的工作原理以及应用知识,属于综合知识的考查,综合性强,难度适中.

练习册系列答案
相关题目
居室装修用石材的放射性常用
Ra作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖.下列叙述中正确的是( )
88 22 |
A、一个
| ||
| B、Ra元素位于元素周期表中第六周期ⅡA族 | ||
| C、RaCl2难溶于水 | ||
| D、Ra(OH)2是一种两性氢氧化物 |
下列物质按纯净物、混合物、强电解质、弱电解质、非电解质的组合中,正确的是( )
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 醋酸 | HD |
| B | 冰醋酸 | 福尔马林 | 苛性钾 | HI | 乙醇 |
| C | 火碱 | 蔗糖溶液 | 氯化钠 | 氨水 | 三氧化硫 |
| D | 胆矾 | 石灰水 | 硫酸钡 | HNO2 | NH3 |
| A、A、 | B、B、 | C、C、 | D、D、 |
根据下列化学方程式判断物质氧化性或还原性强弱排序正确的是( )
①2FeCl3+Cu=2FeCl2+CuCl2 ②CuCl2+Fe=FeCl2+Cu.
①2FeCl3+Cu=2FeCl2+CuCl2 ②CuCl2+Fe=FeCl2+Cu.
| A、还原性:Fe>Cu>FeCl2 |
| B、还原性:Fe>FeCl2>Cu |
| C、氧化性:CuCl2>FeCl3>FeCl2 |
| D、氧化性:FeCl3>FeCl2>CuCl2 |
实验室制Cl2反应为4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O下列说法不正确的是( )
| ||
| A、还原剂是浓HCl,氧化剂是MnO2 |
| B、每生成1mol Cl2,转移电子2mol |
| C、每消耗1mol MnO2,浓HCl被还原4mol |
| D、转移1mol电子时,生成的Cl2在标准状况下体积为11.2 L |