题目内容
下列各组物质的性质比较中,正确的是( )
| A、酸性:HClO4>H3PO4>H2SO4 |
| B、氢化物的稳定性:H2S>HF>H2O |
| C、碱性:Al(OH)3>Mg(OH)2>NaOH |
| D、氧化性:F2>C12>Br2>I2 |
考点:同一周期内元素性质的递变规律与原子结构的关系,同一主族内元素性质递变规律与原子结构的关系
专题:
分析:A.非金属性越强,最高价含氧酸的酸性越强;
B.非金属性越强,氢化物越稳定;
C.金属性越强最高价氧化物对应水化物的碱性越强;
D.非金属性越强,对应单质的氧化性越强.
B.非金属性越强,氢化物越稳定;
C.金属性越强最高价氧化物对应水化物的碱性越强;
D.非金属性越强,对应单质的氧化性越强.
解答:
解:A.同周期自左而右非金属性增强,非金属性越强最高价含氧酸的酸性越强,酸性:HClO4>H2SO4>H3PO4,故A错误;
B.同主族自上而下非金属性减弱,同周期自左而右非金属性增强,故非金属性F>O>S,非金属性越强氢化物越稳定,故稳定性HF>H2O>H2S,故B错误;
C.同周期自左而右金属性减弱,金属性越强最高价氧化物对应水化物的碱性越强,故碱性:NaOH>Mg(OH)2>Al(OH)3,故C错误;
D.同主族自上而下非金属性减弱,非金属性越强,对应单质的氧化性越强,则化性:F2>C12>Br2>I2,故D正确;
故选D.
B.同主族自上而下非金属性减弱,同周期自左而右非金属性增强,故非金属性F>O>S,非金属性越强氢化物越稳定,故稳定性HF>H2O>H2S,故B错误;
C.同周期自左而右金属性减弱,金属性越强最高价氧化物对应水化物的碱性越强,故碱性:NaOH>Mg(OH)2>Al(OH)3,故C错误;
D.同主族自上而下非金属性减弱,非金属性越强,对应单质的氧化性越强,则化性:F2>C12>Br2>I2,故D正确;
故选D.
点评:本题考查同周期同主族性质递变规律,题目难度不大,注意规律的掌握理解,侧重于基本规律应用的考查.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
烷烃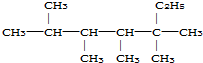 是由烯烃R和氢气发生加成反应后的产物,则R可能的结构有( )
是由烯烃R和氢气发生加成反应后的产物,则R可能的结构有( )
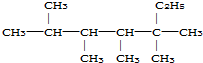 是由烯烃R和氢气发生加成反应后的产物,则R可能的结构有( )
是由烯烃R和氢气发生加成反应后的产物,则R可能的结构有( )| A、4种 | B、5种 | C、6种 | D、10种 |
对于复分解反应:X+Y=Z+W,下列叙述正确的( )
| A、若Z是强酸,则X或Y必有一种是酸 |
| B、若Y是强碱,X是盐,则Z或W必有一种是弱碱 |
| C、若W是弱碱,Z是盐,则X或Y必有一种是强碱 |
| D、若X是强酸,Y是盐,反应后可能有强酸或弱酸生成 |
在下列叙述中,能论证盐酸是强酸,醋酸是弱酸的是( )
| A、将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,醋酸所加的水量少 |
| B、盐酸和醋酸都可用相应的钠盐和浓硫酸反应制取 |
| C、相同pH的等体积盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸pH变大,盐酸pH不变 |
| D、相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
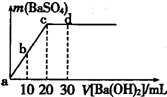 常温下,向0.25mol/L的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是( )
常温下,向0.25mol/L的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是( )| A、溶液的pH:a<b<c<d |
| B、溶液的导电能力:a>b>d>c |
| C、a、b溶液呈酸性 |
| D、c、d溶液呈碱性 |
下列不能发生丁达尔效应的分散系是( )
| A、水 | B、雾 |
| C、石灰水 | D、氢氧化铁胶体 |
NA代表阿伏伽德罗常数值,下列说法正确的是( )
| A、在1L0.1mol/L Na2SO3溶液中,离子总数小于0.3NA |
| B、向FeI2溶液中通入氯气,当有2molFe2+被氧化,转移电子的数目为2NA |
| C、常温常压下,46g液态N2O4中含有的分子数为0.5NA |
| D、1mol Na2O和Na2O2混合物中含有阴、阳离子总数是NA |
已知m1g气体A与m2g气体B所含的分子数相等,下列说法中正确的是( )
A、1个A分子的质量是1个B分子的质量的
| ||
B、同温同体积等质量的A与B的压强之比为
| ||
C、同温同质量的A与B的分子数之比为
| ||
D、同温同压下A与B的密度之比为
|