��Ŀ����
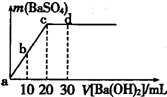 �����£���0.25mol/L��������Һ����μ������ʵ���Ũ����ͬ������������Һ�����ɳ����������������������Һ�������ϵ��ͼ��ʾ��a��b��c��d�ֱ��ʾʵ��ʱ��ͬ�ε���Һ�������й�˵���в���ȷ���ǣ�������
�����£���0.25mol/L��������Һ����μ������ʵ���Ũ����ͬ������������Һ�����ɳ����������������������Һ�������ϵ��ͼ��ʾ��a��b��c��d�ֱ��ʾʵ��ʱ��ͬ�ε���Һ�������й�˵���в���ȷ���ǣ�������| A����Һ��pH��a��b��c��d |
| B����Һ�ĵ���������a��b��d��c |
| C��a��b��Һ������ |
| D��c��d��Һ�ʼ��� |
���㣺�������Һ�ĵ�����,���ӷ�Ӧ����������
ר�⣺
���������������������Ӧ����ʽΪBa2++2OH-+SO42-+2H+=BaSO4��+2H2O�����ݷ���ʽ֪�����ŷ�Ӧ�Ľ��У���Һ������Ũ����Сֱ������ȫ��Ӧ��
A��������Һ�����ԣ��������������ļ��룬��Һ��������Ũ����С��pH������
B����Һ��������������Ũ�ȳ����ȣ�
C��������Һ�����ԣ��������������ļ��룬��Һ��������Ũ����С�����Լ�����
D��c�����ǡ�÷�Ӧ�������ᱵ��ˮ��d����������������
A��������Һ�����ԣ��������������ļ��룬��Һ��������Ũ����С��pH������
B����Һ��������������Ũ�ȳ����ȣ�
C��������Һ�����ԣ��������������ļ��룬��Һ��������Ũ����С�����Լ�����
D��c�����ǡ�÷�Ӧ�������ᱵ��ˮ��d����������������
���
�⣺���������������Ӧ����ʽΪBa2++2OH-+SO42-+2H+=BaSO4��+2H2O�����ݷ���ʽ֪�����ŷ�Ӧ�Ľ��У���Һ������Ũ����Сֱ������ȫ��Ӧ��
A��������Һ�����ԣ��������������ļ��룬��Һ��������Ũ����С��pH������������Һ��pH��a��b��c��d����A��ȷ��
B����Һ��������������Ũ�ȳ����ȣ���Һ������Ũ���ȼ�С������������Һ���������ȼ�С��������Һ��������Ϊa��b��d��c����B��ȷ��
C��������Һ�����ԣ��������������ļ��룬��Һ��������Ũ����С�����Լ�����a��b��������������Һ�����ԣ���C��ȷ��
D��c�����ǡ�÷�Ӧ�������ᱵ��ˮ��d��������������������c��Һ�����ԡ�d��Һ�ʼ��ԣ���D����
��ѡD��
A��������Һ�����ԣ��������������ļ��룬��Һ��������Ũ����С��pH������������Һ��pH��a��b��c��d����A��ȷ��
B����Һ��������������Ũ�ȳ����ȣ���Һ������Ũ���ȼ�С������������Һ���������ȼ�С��������Һ��������Ϊa��b��d��c����B��ȷ��
C��������Һ�����ԣ��������������ļ��룬��Һ��������Ũ����С�����Լ�����a��b��������������Һ�����ԣ���C��ȷ��
D��c�����ǡ�÷�Ӧ�������ᱵ��ˮ��d��������������������c��Һ�����ԡ�d��Һ�ʼ��ԣ���D����
��ѡD��
���������������������������ӦΪ���忼����ҺpH�仯����Һ�����Ա仯��֪ʶ�㣬��ȷÿһ����Һ�е������ǽⱾ��ؼ���ע����Һ��������������Ũ�ȳ����ȣ�������ǿ���أ�Ϊ�״��㣮

��ϰ��ϵ�д�
�����Ŀ
���������ڹ�������������Ӧ��ֻ����һ��һ�ȴ������ǣ�������
| A�������� | B���춡�� |
| C�������� | D�������� |
20mL0.1mol/L������40mL0.05mol/L����������Һ��ϣ���������Һ�У�������
| A��c��Na+����c��CH3COO-����c��OH-����c��H+�� |
| B��c��Na+����c��CH3COO-����c��H+����c��OH-�� |
| C��c��Na+����c��CH3COO-����c��H+��=c��OH-�� |
| D��c��Na+��=c��CH3COO-����c��OH-����c��H+�� |
���и�װ���У����ܹ���ԭ��ص��ǣ�����ʶ�Ϊϡ���ᣩ��������
A��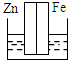 |
B��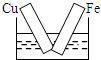 |
C�� |
D��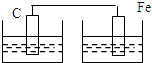 |
���и������ʵ����ʱȽ��У���ȷ���ǣ�������
| A�����ԣ�HClO4��H3PO4��H2SO4 |
| B���⻯����ȶ��ԣ�H2S��HF��H2O |
| C�����ԣ�Al��OH��3��Mg��OH��2��NaOH |
| D�������ԣ�F2��C12��Br2��I2 |
�Ȼ�ѧ����ʽC��s��+H2O��g���TCO��g��+H2��g����H=+131.3kJ/mol��ʾ��������
| A��̼��ˮ��Ӧ����131.3kJ���� |
| B��1mol̼��1molˮ��Ӧ����һ����̼������������131.3kJ���� |
| C��1mol��̬̼��1molˮ������Ӧ����һ����̼�����������������131.3kJ |
| D��1����̬̼ԭ�Ӻ�1��ˮ�������ӷ�Ӧ����131.1kJ |
��NAΪ�����ӵ�����������˵���У���ȷ���ǣ�������
| A��2L1mol/LNa2SO4��Һ�к��е���������Ϊ3NA |
| B��16 g CH4����ԭ����ĿΪNA |
| C��18g NH4+������������ĿΪ11NA |
| D��18 gˮ����������ĿΪNA |