题目内容
4. 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.
已知:①N2(g)+O2(g)═2NO(g)△H1=+180.5kJ•mol-1
②C和CO的燃烧热(△H)分别为-393.5kJ•mol-1和-283kJ•mol-1
则2NO(g)+2CO(g)═N2(g)+2CO2(g)的△H=-746.5kJ•mol-1
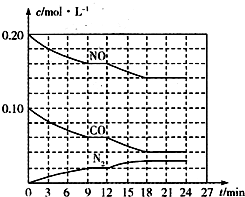
(2)将0.20mol NO和0.10mol CO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示.
①CO在0-9min内的平均反应速率v(CO)=4.4×10-3 mol•L-1•min-1 (保留两位有效数字);第12min时改变的反应条件可能为D.
A.升高温度 B.加入NOC.加催化剂 D.降低温度
②该反应在第24min时达到平衡状态,CO2的体积分数为22.2%(保留三位有效数字),化学平衡常数K=3.4L/mol(保留两位有效数字).
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=2c(SO
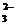 )+c(HSO
)+c(HSO )(用含硫微粒浓度的代数式表示).
)(用含硫微粒浓度的代数式表示).(4)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2.已知常温下0.1mol•L-1的HCOONa溶液pH=10,则HCOOH的电离常数Ka=1.0×10-7.
分析 (1)写出C和CO燃烧热的热化学方程式,结合盖斯定律计算所需要的热化学方程式;
(2)①分析图象浓度变化,结合反应速率概念计算V=$\frac{△c}{△t}$得到,第12min时一氧化碳和一氧化氮减小,氮气浓度增大,说明平衡正向进行,依据化学平衡移动原理分析判断选项对平衡的影响;
②依据图象分析判断,平衡状态时一氧化碳一氧化氮和氮气浓度,结合化学平衡三段式列式计算平衡百分含量和平衡常数;
(3)依据溶液中存在的电荷守恒分析;
(4)计算水解平衡常数Kh,再根据Ka=$\frac{Kw}{Kh}$计算.
解答 解:(1)①N2(g)+O2(g)═2NO(g)△H1=+180.5kJ•mol-1
②C的燃烧热(△H)为-393.5kJ•mol-1,热化学方程式为C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1;
③C0的燃烧热283kJ•mol-1 ,热化学方程式为CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283kJ•mol-1;
依据盖斯定律计算③×2-①得到,2NO(g)+2CO(g)═N2(g)+2CO2(g)的△H=-746.5KJ/mol
故答案为:-746.5;
(2)①图象分析一氧化碳浓度变化=0.10mol/L-0.06mol/L=0.04mol/L,CO在0-9min内的平均反应速率v(CO)=$\frac{0.04mol/L}{9min}$=4.4×10-3,第12min时,一氧化碳和一氧化氮浓度减小,浓度增大说明平衡正向进行;
A.反应是放热反应,升高温度,平衡逆向进行,故A不符合;
B.加入NO,平衡正向进行,一氧化氮浓度大于原平衡,故B不符合;
C.加催化剂改变反应速率不改变化学平衡,故C不符合;
D.反应是放热反应,降低温度,平衡正向进行,故D符合;
改变的反应条件可能是降低温度;
故答案为:4.4×10-3;D;
②该反应在第24min时达到平衡状态,平衡浓度c(N2)=0.03mol/L,c(NO)=0.14mol/L,c(CO)=0.04mol/L,依据化学平衡三段式列式计算
2NO(g)+2CO(g)═N2(g)+2CO2(g)
起始量(mol/L) 0.2 0.1 0 0
变化量(mol/L) 0.06 0.06 0.03 0.06
平衡量(mol/L) 0.14 0.04 0.03 0.06
CO2的体积分数=$\frac{0.06}{0.14+0.04+0.03+0.06}$×100%=22.2%
平衡常数K=$\frac{0.0{6}^{2}×0.03}{0.1{4}^{2}×0.0{4}^{2}}$=3.4
故答案为:22.2%;3.4;
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,依据溶液中电荷守恒分析,c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-),c(H+)=c(OH-),得到(Na+)=2c(SO32-)+c(HSO3-),故答案为:2c(SO32-)+c(HSO3-);
(4)常温下,0.1mol/L的HCOONa溶液pH为10,溶液中存在HCOO-水解HCOO-+H2O?HCOOH+OH-,故Kh=$\frac{1{0}^{-4}×1{0}^{-4}}{0.1-1{0}^{-4}}$=10-7,则HCOOH的电离常数Ka=$\frac{Kw}{Kh}$=$\frac{1{0}^{-14}}{1{0}^{-7}}$=1×10-7,故答案为:1.0×10-7.
点评 本题考查了热化学方程式书写方法,化学平衡建立,平衡状态影响因素分析,化学反应速率、平衡常数计算应用,电解质溶液电荷守恒,弱电解质电离平衡的计算应用,掌握基础是关键,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
| A. | 戊烷 | B. | 戊烯 | C. | 乙酸乙酯 | D. | 丁醇 |
| A. | 制取溴苯:将铁屑、溴水、苯混合加热 | |
| B. | 鉴别己烯和苯:分别向己烯和苯中滴入酸性KMnO4溶液,振荡,观察是否褪色 | |
| C. | 实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 | |
| D. | 检验卤代烃中的卤素原子:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀颜色 |
| A. | 1molS2C12价电子数为66NA | |
| B. | 氧化产物与还原产物的物质的量之比为l:7 | |
| C. | 每生成l mol SO2转移4 NA电子 | |
| D. | 每生成48g硫单质会断裂5NA共价键 |
| A. |  | B. |  | C. |  | D. |  |
| A. | BF3 | B. | PCl5 | C. | NCl3 | D. | CH4 |
| A. | 碘水 | B. | 碘水、烧碱溶液、新制的Cu(OH)2 | ||
| C. | 氢氧化钠溶液、银氨溶液 | D. | 烧碱溶液、新制的Cu(OH)2 |
 ,(2)NH3:
,(2)NH3: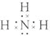 ,
,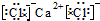 ,(4)CO2:
,(4)CO2: .
.