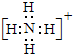题目内容
13.下列分子中,所有原子都满足最外层为8电子结构的是( )| A. | BF3 | B. | PCl5 | C. | NCl3 | D. | CH4 |
分析 对于ABn型共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,含H元素的化合物一定不满足8电子结构.
解答 解:A、BF3中,B元素位于第ⅢA族,则3+3≠8,不满足分子中所有原子都满足最外层8电子结构,故A错误;
B、PCl5中,P原子的最外层电子为:5+5≠8,不满足分子中所有原子都满足最外层8电子结构,故B错误;
C、NCl3中N元素化合价为+3,N原子最外层电子数为5,所以5+3=8,N原子满足8电子结构,Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故C正确;
D、CH4中C元素化合价为+4,Si原子最外层电子数为4,所以4+4=8,C原子满足8电子结构,H原子的最外层电子为:1+1=2,不满足8电子稳定结构,故D错误.
故选:C.
点评 本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列物质中,既有离子键又有共价键的是( )
| A. | MgCl2 | B. | NH4Cl | C. | CO2 | D. | H2S |
1.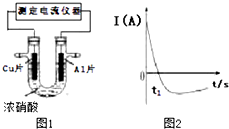 常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(如图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,已知0-t1时,原电池的负极是Al片,反应过程中有红棕色气体产生.下列说法不正确的是( )
常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(如图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,已知0-t1时,原电池的负极是Al片,反应过程中有红棕色气体产生.下列说法不正确的是( )
 常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(如图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,已知0-t1时,原电池的负极是Al片,反应过程中有红棕色气体产生.下列说法不正确的是( )
常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(如图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,已知0-t1时,原电池的负极是Al片,反应过程中有红棕色气体产生.下列说法不正确的是( )| A. | 0-t1时,正极的电极反应式为:2H++NO3--e-═NO2+H2O | |
| B. | 0-t1时,溶液中的H+向Cu电极移动 | |
| C. | t1时,负极的电极反应式为:Cu-2e-═Cu2+ | |
| D. | t1时,原电池中电子流动方向发生改变是因为Al在浓硝酸中钝化,氧化膜阻碍了Al的进一步反应 |
8.下列说法正确的是( )
| A. | 将金属A投入B的盐溶液,A溶解说明A的金属性比B的金属性强 | |
| B. | 用干燥洁净的铂丝蘸取少量待测液在酒精灯火焰上灼烧,火焰呈黄色,说明该溶液是钠盐溶液 | |
| C. | 合成新型农药可以在元素周期表的金属与非金属交界处区域探寻 | |
| D. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2 ml 5%H2O2和1 mlH2O,向另一支试管中加入2 mL 5%H2O2和1 mLFeCl3溶液,观察并比较实验现象 |
18.某化学兴趣小组用铝片与稀硫酸反应制取氢气,以下能够加快该反应速率的是( )
①用18.4mol/L的浓硫酸代替稀硫酸 ②加热 ③改用铝粉 ④增大稀硫酸的体积 ⑤加水
⑥加入少量硫酸铜固体 ⑦加入少量硝酸钠固体.
①用18.4mol/L的浓硫酸代替稀硫酸 ②加热 ③改用铝粉 ④增大稀硫酸的体积 ⑤加水
⑥加入少量硫酸铜固体 ⑦加入少量硝酸钠固体.
| A. | ②③⑥ | B. | 全部 | C. | ①②③⑥⑦ | D. | ②③④⑥⑦ |
2.下列反应中,属于取代反应的是( )
| A. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2 H2O | |
| B. | CH4+2O2$\stackrel{点燃}{→}$CO2+H2O | |
| C. | 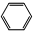 +HO-NO2$→_{△}^{浓硫酸}$ +HO-NO2$→_{△}^{浓硫酸}$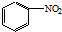 +H2O +H2O | |
| D. | CH2=CH2+H2O$→_{△}^{催化剂}$CH3CH2OH |
3.下列实验方案能达到目的是( )
| A. | 除去NaCl固体中混有的MgCl2:加入KOH试剂后过滤 | |
| B. | 实验室获取少量纯净的水:蒸馏自来水 | |
| C. | 提纯混有少量硝酸钾的氯化钾:将混合物溶于热水中,再冷却、结晶并过滤 | |
| D. | 提取碘水中的碘:加入适量乙醇,振荡、静置、分液 |
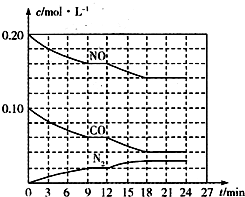 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要. )+c(HSO
)+c(HSO )(用含硫微粒浓度的代数式表示).
)(用含硫微粒浓度的代数式表示).