题目内容
19. (1)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.
(1)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.已知:①N2(g)+2O2(g)=N2O4 (g)△H1=-195kJ•mol-1
②N2H4 (1)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
写出肼和N2O4 反应的热化学方程式2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol;
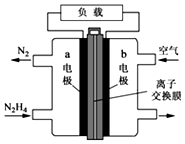
(2)肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景.其工作原理如图所示,回答下列问题:
①该燃料电池的负极发生的反应式为N2H4+4OH--4e-=N2+4H2O.
②电池工作时,OH-移向a极(“a”或“b”)
③当电池放电转移5mol电子时,至少消耗燃料肼40g.
(3)LiCoO2可用作一种锂离子电池的正极材料.该锂离子电池充电过程中,负极发生的反应为6C+xLi++xe-═LixC6,正极发生LiCoO2与Li1-xCoO2之间的转化,写出放电时电池总反应方程式Li1-xCoO2+LixC6═6C+LiCoO2.
分析 (1)根据盖斯定律,②×2-①可得目标热化学方程式;
(2)①燃料电池的正极是氧气在正极发生还原反应,是负极发生氧化反应,是肼在反应,注意电解质溶液的酸碱性即可;
②原电池中阴离子移向负极;
③据负极电极反应式计算消耗燃料肼的质量.
(3)结合电极方程式以及两极的变化,判断反应物和生成物,可书写总方程式.
解答 解:(1)肼可作为火箭发动机的燃料,与氧化剂N2H4反应生成N2和水蒸气,将方程式②×2-①得肼和N2H4 反应的热化学方程式2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol,
故答案为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol;
(2)①燃料电池的正极是氧气在正极发生还原反应,负极发生氧化反应,是肼在反应,肼中的N从-2价升高到0价,碱性电池中,其电极反应式应为:N2H4+4OH--4e-=N2+4H2O,
故答案为:N2H4+4OH--4e-=N2+4H2O;
②原电池中阴离子移向负极,a为负极,所以电池工作时,OH-移向a电极,故答案为:a;
③负极电极反应式为N2H4+4OH--4e-=4H2O+N2↑,转移4mol电子时消耗肼32g,则转移5mol电子消耗肼32g×$\frac{5}{4}$=40g,故答案为:40;
(3)放电时,负极反应为:LixC6-xe-═6C+xLi+,正极Li1-xCoO2+xLi++xe-=LiCoO2,总电池反应方程式为:Li1-xCoO2+LixC6═6C+LiCoO2,
故答案为:Li1-xCoO2+LixC6═6C+LiCoO2.
点评 本题考查较为综合,为高频考点,侧重于学生的分析、计算能力的考查,题目涉及盖斯定律、电极反应式以及电池反应方程式书写,题目难度较大.

| A. | 加大盐酸用量 | B. | 减小盐酸浓度 | C. | 粉碎石灰石 | D. | 增大体系压强 |
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g)$\stackrel{Ru}{?}$CH4(g)+2H2O(g)
已知H2的体积分数随温度的升高而增加.若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化.(填“增大”、“减小”或“不变”)
| v正 | v逆 | 平衡常数K | 转化率α |
| [CO2]/mol•L-1 | [H2]/mol•L-1 | [CH4]/mol•L-1 | [H2O]/mol•L-1 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
(3)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5 0.1mol/L Na2CO3溶液的pH>0.1mol/L Na2C2O4溶液的pH.(选填“大于”“小于”或“等于”)
等浓度草酸溶液和碳酸溶液中,氢离子浓度较大的是草酸.
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是ac.(选填编号)
a.[H+]>[HC2O4-]>[HCO3-]>[CO32-]b.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
c.[H+]>[HC2O4-]>[C2O42-]>[CO32-]d.[H2CO3]>[HCO3-]>[HC2O4-]>[CO32-].
| A. |  3-甲基-2-乙基戊烷 3-甲基-2-乙基戊烷 | |
| B. | (CH3)3CCH2CH(C2H5)CH3 2,2-二甲基-4-乙基戊烷 | |
| C. |  邻甲基苯酚 邻甲基苯酚 | |
| D. |  2-甲基-3-戊炔 2-甲基-3-戊炔 |
| A. | 称量时托盘上要垫上干净的称量纸 | |
| B. | 移液时不慎有部分液体溅出,会造成所配溶液浓度偏小 | |
| C. | 定容时俯视容量瓶刻度线,会造成所配溶液浓度偏大 | |
| D. | 定容摇匀后发现液面下降,不应再加蒸馏水 |
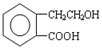 ,它可通过不同化学反应分别制得B、C和D 三种物质.
,它可通过不同化学反应分别制得B、C和D 三种物质.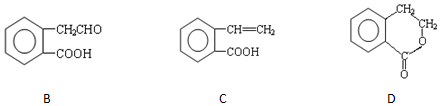
 +H2O
+H2O
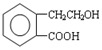 .
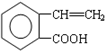
.

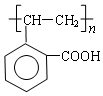 .
.