题目内容
11.下列气体中,既能用碱石灰干燥,又能用排水法收集的是( )| A. | CO | B. | NO2 | C. | SO2 | D. | NH3 |
分析 能用碱石灰干燥,说明该气体不与氢氧根离子反应,为中性或碱性气体;能用排水法收集,说明该气体不与水反应或不易溶于水,据此结合选项中气体的性质进行解答.
解答 解:A.CO为中性气体,不与碱石灰反应,能够用碱石灰干燥,且CO不溶于水,也不与水反应,能够用排水法收集,故A正确;
B.NO2能够与水反应生成NO和硝酸,不能用排水法收集,故B错误;
C.SO2易溶于水,能够与碱石灰反应,不能用排水法收集,也不能用碱石灰干燥,故C错误;
D.NH3极易溶于水,不能用排水法收集,故D错误;
故选A.
点评 本题考查了常见气体的干燥、收集方法,题目难度不大,明确常见气体的性质为解答关键,注意掌握常见气体的收集、干燥方法,试题培养了学生的灵活应用能力.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
1.用石墨做电极电解下列溶液,通电一段时间后溶液的pH变大的是( )
| A. | NaCl溶液 | B. | NaOH溶液 | C. | H2SO4溶液 | D. | CuSO4溶液 |
2.对下列实验现象的原因分析不正确的一项是( )
| 选项 | 实验现象 | 原因分析 |
| A | 浓硫化钠溶液有臭味 | 硫离子水解生成硫化氢,硫化氢具有臭味 |
| B | 新制氯水中滴加石蕊试液,溶液先变红,后褪色 | 氯气与水反应生成HCl、HClO,HCl显强酸性,使石蕊变红,HClO具有强氧化性,使其褪色 |
| C | SO 2通入溴水中,溴水褪色 | SO 2具有漂白性,使其褪色 |
| D | 向饱和Na2CO3溶液中通入足量CO2气体,溶液变浑浊 | 析出了NaHCO3晶体 |
| A. | A | B. | B | C. | C | D. | D |
19.下列微粒半径大小顺序正确的是( )
| A. | O2->F->Na+>Mg2+ | B. | Na>Mg>Cl>Ar | C. | I>Br>F>Cl | D. | Na>Na+>S2->S |
6.某原电池总反应的离子方程式为 2Fe3++Fe=3Fe2+,能实现该反应的原电池是( )
| A. | 正极为 Cu,负极为 Fe,电解质为 FeCl3 溶液 | |
| B. | 正极为Fe,负极为Zn,电解质为 Fe(NO3)3 溶液 | |
| C. | 正极为 Fe,负极为 Zn,电解质为 FeSO4 溶液 | |
| D. | 正极为 Ag,负极为 Fe,电解质为 CuSO4 溶液 |
16.下列反应不属于取代反应的是( )
| A. | 甲苯与氯气在光照条件下反应 | B. | 甲苯与液溴在铁催化作用下反应 | ||
| C. | 乙酸乙酯在碱性条件下水解 | D. | 乙醇制备乙醛 |
3.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 1molCl2 与过量乙烷在光照下反应,生成的有机物中含有氯原子的总数为2NA | |
| B. | 1molC3H8 中含有的共用电子对数为11NA | |
| C. | 1.5g 甲基含有的质子数和电子数之和为1.8NA | |
| D. | 标况下,11.2 L癸烷含有的原子个数为16 NA |
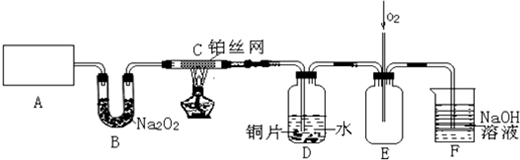
 氮元素可形成卤化物、叠氮化物及络合物等.
氮元素可形成卤化物、叠氮化物及络合物等.