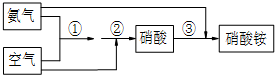
题目内容
7. 氮元素可形成卤化物、叠氮化物及络合物等.
氮元素可形成卤化物、叠氮化物及络合物等.(1)NF3构型为三角锥体,沸点-129℃;可在铜催化作用下由F2和过量NH3反应得到.NF3属于分子晶体,写出制备 NF3的化学反应方程式:3F2+4NH3$\frac{\underline{\;Cu\;}}{\;}$NF3+3NH4F.
(2)氢叠氮酸(HN3)是一种弱酸,它的酸性类似于醋酸,微弱电离出H+和N3-.
①与N3-互为等电子体的分子、离子有:CO2、SCN-(各举1例),由此可推知N3-的空间构型是直线型.
②叠氮化物、氰化物能与Fe3+及Cu2+及Co3+等形成络合物,如:Co[(N3)(NH3)5]SO4、(Fe(CN)64-.写出钴原子在基态时的价电子排布式:3d74s2.Co[(N3)(NH3)5]SO4中钴的配位数为6,CN-中C原子的杂化类型是sp.
(3)化学式为Pt(NH3)2Cl2的化合物有两种异构体,其中一种异构体具有水的可溶性,则此种化合物是极性(填“极性”、“非极性”)分子.
(4)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)=2Na(l)+3N2(g),有关说法正确的是BC (选填序号)
A.NaN3与KN3结构类似,前者晶格能较小
B.第一电离能(I1):N>P>S
C.钠晶胞结构如图,该晶胞分摊2个钠原子
D.氮气常温下很稳定,是因为氮的电负性小.
分析 (1)NF3的沸点-129℃,符合分子晶体的性质;在铜催化作用下F2和过量NH3反应得到NF3,还生成NH4F;
(2)①原子总数相等、价电子总数也相等的微粒互为等电子体,等电子体的结构相似;
②钴原子核外电子数为27,根据能量最低原理书写基态时的价电子排布式;
[Co(N3)(NH3)5]SO4中配体为N3-、NH3;
CN-中C原子价层电子对数=1+$\frac{4+1-3}{2}$=2,杂化轨道数目为2;
(3)根据相似相溶原理,极性分子易溶于极性溶剂;
(4)A.离子半径越小,晶格能越大;
B.同主族自上而下第一电离能减小,P元素原子3p轨道为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的;
C.钠晶胞结构为体心立方密堆积,根据均摊法计算晶胞中分摊钠原子数目;
D.氮气性质稳定是由于氮气分子中含有氮氮三键.
解答 解:(1)NF3的沸点-129℃,沸点很低,属于分子晶体.在铜催化作用下F2和过量NH3反应得到NF3,还生成NH4F,反应方程式为:3F2+4NH3$\frac{\underline{\;Cu\;}}{\;}$NF3+3NH4F,
故答案为:分子;3F2+4NH3$\frac{\underline{\;Cu\;}}{\;}$NF3+3NH4F;
(2)①与N3-互为等电子体的微粒含有3个原子、16个价电子,与其等电子体的分子有N2O或CO2或CS2或BeCl2等,其等电子体的离子有 SCN-等;
N3-与CO2是等电子体,具有相同的价电子数,它们具有相似的化学结构,二氧化碳是直线型分子,所以N3-的空间构型是直线形,
故答案为:CO2;SCN-;直线;
②钴原子核外电子数为27,其基态原子核外电子排布式为1s22s22p63s23p63d74s2,价电子排布式为3d74s2,
[Co(N3)(NH3)5]SO4中配体为N3-、NH3,钴的配位数为6,
CN-中C原子价层电子对数=1+$\frac{4+1-3}{2}$=2,杂化轨道数目为2,C原子采取sp杂化;
故答案为:3d74s2;6;sp;
(3)极性分子易溶于极性溶剂中,水为极性溶剂,Pt(NH3)2Cl2的一种分子易溶于水,说明为极性分子;
故答案为:极性;
(4)A.离子电荷相同,钠离子半径小于钾离子半径,故NaN3的晶格能大于KN3的晶格能,故A错误;
B.同主族自上而下第一电离能减小,P元素原子3p轨道为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的,故第一电离能N>P>S,故B正确;
C.钠晶胞结构为体心立方密堆积,晶胞中原子数为1+8×$\frac{1}{8}$=2,故C正确;
D.氮气分子中含有氮氮三键,键能较大,所以性质稳定,故D错误.
故选:BC.
点评 本题是对物质结构与性质的考查,涉及晶体类型与性质、核外电子排布、等电子体、配合物、杂化方式与空间构型、晶胞计算、电离能等,需要学生具备扎实的基础,注意同周期主族元素第一电离能异常情况.

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案| A. | CO | B. | NO2 | C. | SO2 | D. | NH3 |
| A. | 0.288g | B. | 0.366g | C. | 0.384g | D. | 0.396g |

(1)工业生产中产生的含SO2废气经石灰吸收和氧化后制成硫酸钙,写出反应方程式2SO2+2Ca(OH)2+O2=2CaSO4+2H2O.
(2)装置Ⅱ中,在一定条件下,二氧化硫和氧气发生反应时,温度与二氧化硫的转化率的关系如表所示:
| 温度/℃ | 400 | 500 | 600 |
| SO2转化率/% | 99.2 | 93.5 | 73.7 |
②关于此反应下列说法正确的是ac(填字母).
a.该反应△H<0
b.反应达到平衡时,SO2,O2,SO3 的浓度一定都相等
c.反应达到平衡状态时,v(SO2)正=2v(O2)逆
d.升高温度或使用催化剂都可提高SO2的转化率
③硫酸厂尾气(主要成分为SO2、O2和N2)中低浓度SO2的吸收有很多方法.用氨水吸收上述尾气,若尾气中
SO2与氨水恰好反应得到弱碱性的(NH4)2SO3溶液,则有关该溶液的下列关系正确的是ac (填字母).
a.c(NH4+)+c(NH3•H2O)=2[c(SO32-)+c(HSO3-)+c(H2SO3)]
b.c(NH4+)+c (H+)=c (SO32-)+c (HSO3-)+c (OH-)
c.c(NH4+)>c (SO32-)>c (OH-)>c (H+)
(3)装置Ⅲ中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO).
已知:①2CO(g)+O2(g)═2CO2(g)△H=-283kJ•mol-1
②2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
③2CH3OH(l)+3O2(g)═2CO2(g)+4H2O (l)△H=-725.8kJ•mol-1
试写出CO与H2在一定条件下反应生成CH3OH(l)的热化学方程式CO(g)+2H2(g)=CH3OH(l)△H=-350.2kJ•mol-1.
(4)在固态金属氧化物电解池中,一定条件下H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图2所示.
①Y端是电源的正极(填正极或负极).
②阴极的电极反应式为 CO2+2eˉ=CO+O2ˉ和H2O+2e-═H2↑+O2-.
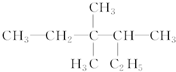 的正确命名为( )
的正确命名为( )| A. | 3,3二甲基4乙基戊烷 | B. | 3,3,4三甲基己烷 | ||
| C. | 2乙基3,3二甲基4乙基戊烷 | D. | 3,4,4三甲基己烷 |
| A. | ⅠA族元素的金属性比ⅡA族元素的金属性强 | |
| B. | 第三周期元素的离子半径从左到右逐渐减小 | |
| C. | 同周期非金属氧化物对应的水化物的酸性从左到右依次增强 | |
| D. | ⅣA族元素的氢化物中,稳定性最好的是CH4 |
 某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步: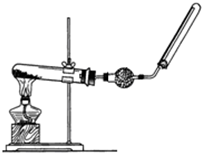 实验室中若用如图所示的装置制取并收集干燥的氨气.
实验室中若用如图所示的装置制取并收集干燥的氨气.