题目内容
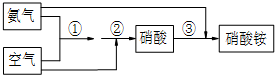
20.某化学兴趣小组在实验室探究氨的有关性质,设计了下图所示实验,A处是气体发生装置,A中所用的实验药品从下列物质中选取.①Na2CO3 ②NaOH ③Ca(OH)2 ④NaHCO3 ⑤NH4Cl
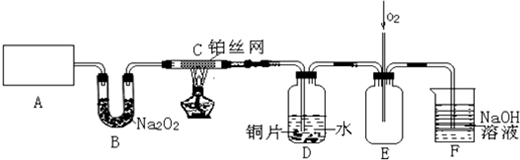
按如图连接好各仪器,现将C处的铂丝网加热至红热,再将A处产生的气体通过B装置片刻后撤去C处酒精灯.部分实验的现象如下:铂丝继续保持红热状态,D中的铜片慢慢溶解,回答下列问题:
(1)A中发生的化学反应方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.制取气体所用到的玻璃仪器主要有2种(不包括连接装置).
(2)B装置的作用为吸收水蒸气并产生氧气.
(3)撤去C处酒精灯后铂丝能继续保持红热状态的原因是该反应为放热反应,为了使D中Cu片溶解的速率加快,可向D处的溶液中加入下列少量物质中的BC(填下列各项序号)
A.Na2CO3 B.AgNO3 C.H2SO4 D.FeSO4
(4)图E中持续通入氧气的作用为将产生的NO氧化,充分被NaOH溶液吸收.
(5)有人认为他们设计的这套实验装置还存在明显的不足,对其不足之处以及应如何改进:CD之间加一个防倒吸的装置.
分析 (1)实验室用加热氯化铵和氢氧化钙混合物的方法制备氨气,反应为固体与固体混合加热,用到的玻璃仪器主要为试管和酒精灯;
(2)B装置作用是吸收水蒸气生成氧气;
(3)放热反应开始后,不需要持续加热;硝酸根离子在酸性环境下具有强的氧化性能够氧化铜,增大氢离子浓度能使Cu片溶解的速率加快,可以加入试剂形成原电池加快反应速率,增大离子浓度加快反应速率;
(4)持续通入氧气使一氧化氮气体全部氧化,被氢氧化钠溶液吸收,减少环境污染;
(5)D装置中的液体易发生倒吸,需要在CD之间加一个防倒吸的装置.
解答 解:(1)加热氯化铵和氢氧化钙混合物生成氯化钙、氨气和水,化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;反应为固体与固体加热,用到的玻璃仪器主要为试管和酒精灯2种;
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;2;
(2)B装置是利用过氧化钠吸收氯化铵和氢氧化钙反应生成的水蒸气生成氧气,
故答案为:吸收水蒸气并产生氧气;
(3)撤去C处酒精灯后铂丝能继续保持红热状态,说明该反应为放热反应;
A.Na2CO3 消耗硝酸不能加快铜的反应速率,故A错误;
B.AgNO3 和铜反应生成银,铜和银在稀硝酸溶液中析出原电池加快反应速率,故B正确;
C. H2SO4 会增大氢离子浓度加快铜与稀硝酸的反应速率,故C正确;
D.FeSO4有还原性会消耗硝酸,所以不能加快铜的反应速率,故D错误;
故答案为:BC;
(4)持续通入氧气使一氧化氮气体全部氧化,被氢氧化钠溶液吸收,减少环境污染,故答案为:将产生的NO氧化,充分被NaOH溶液吸收;
(5)D装置中的液体易发生倒吸到C装置,需要在CD之间加一个防倒吸的装置,故答案为:CD之间加一个防倒吸的装置.
点评 本题考查了氨气的制备、性质的检验,熟悉氨气制备原理是解题关键,注意实验装置的作用和注意问题,题目难度中等.

| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
| A. | CO | B. | NO2 | C. | SO2 | D. | NH3 |
 某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步: