题目内容
9.下列反应中不可能设计成原电池的是( )| A. | NaOH+HCl═NaCl+H2O | B. | 2Fe3++Fe═3Fe2+ | ||
| C. | Zn+2HCl═ZnCl2+H2↑ | D. | 4Al+3O2+6H2O═4Al(OH)3↓ |
分析 能够设计成原电池的反应必须属于自发进行的氧化还原反应,据此根据各选项中是否存在化合价变化进行判断.
解答 解:A.NaOH+HCl═NaCl+H2O为中和反应,不属于氧化还原反应,不能设计成原电池,故A正确;
B.2Fe3++Fe═3Fe2+为自发进行的氧化还原反应,能够设计成原电池,故B错误;
C.Zn+2HCl═ZnCl2+H2↑为置换反应,属于自发进行的氧化还原反应,能够设计成原电池,故C错误;
D.4Al3O2+6H2O═4Al(OH)3↓为自发进行的氧化还原反应,能够设计成原电池,故D错误;
故选A.
点评 本题考查原电池设计,题目难度不大,明确原电池原理及原电池反应特点是解本题关键,注意原电池反应限制性条件“自发进行、放热、氧化还原反应”,知道常见反应的反应热、常见的氧化还原反应.

练习册系列答案
相关题目
19.鉴别Cl-、Br-、I-可以选用的试剂是( )
| A. | 碘水,淀粉溶液 | B. | 溴水,四氯化碳 | ||
| C. | 淀粉,KI溶液 | D. | 硝酸银溶液,稀HNO3 |
20.井水冒泡、有异味和变浑浊是地震的常见征兆,其中可能涉及地下硫铁矿(FeS2)发生的反应:FeS2+H2O═Q+S+H2S↑ (已配平),则物质Q是( )
| A. | Fe2O3 | B. | FeO | C. | Fe(OH)2 | D. | Fe(OH)3 |
17.下列各项实验操作中,正确的是( )
| A. | 用氨水洗涤试管内壁上的“银镜” | |
| B. | 只用溴水鉴别苯、CCH4、KI溶液、Na2SO4溶液 | |
| C. | 为加快过滤速度,用玻璃棒搅拌过滤器中的食盐水 | |
| D. | 为迅速除去乙酸乙酯中的少量乙酸,加入足量NaOH溶液并加热 |
4.氢核磁共振谱是根据不同化学环境的氢原子在谱中给出的信号不同来确定有机物分子中氢原子种类的.下列有机物分子中,在氢核磁共振谱中只给出一种信号的是( )
| A. | 丙烷 | B. | 新戊烷 | C. | 正丁烷 | D. | 异丁烷 |
14.下列说法错误的是( )
| A. | 0.1mol/LCH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L | |
| B. | Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S) | |
| C. | 配制FeCl3溶液,应加少量盐酸 | |
| D. | 将Al2(SO4)3溶液蒸干,灼烧得Al2O3 |
18.下列关于氯水的说法中,不正确的是( )
| A. | 氯水是指氯气的水溶液 | |
| B. | 在pH试纸上滴新制氯水,试纸会先变红后褪色 | |
| C. | 久置的氯水漂白作用更强 | |
| D. | 新制氯水应避光保存 |
19.当温度不变时,恒容的容器中进行反应2A?B,若反应物的浓度由0.1mol•L-1降到0.06mol•L-1需20秒,那么由0.06mol•L-1降到0.036mol•L-1,所需反应的时间为( )
| A. | 等于10秒 | B. | 等于12秒 | C. | 大于12秒 | D. | 小于12秒 |
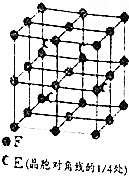 A、B、C、D、E、F为元素周期表前四周期元素且原子序数依次增大,A的基态原子有3个不同的能级,各能级中电子数相等;B2-、C-、D+、E3+具有相同的电子构型;D元素的焰色反应呈黄色;F的基态原子的价电子排布式为3d64s2.
A、B、C、D、E、F为元素周期表前四周期元素且原子序数依次增大,A的基态原子有3个不同的能级,各能级中电子数相等;B2-、C-、D+、E3+具有相同的电子构型;D元素的焰色反应呈黄色;F的基态原子的价电子排布式为3d64s2.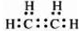 .
.