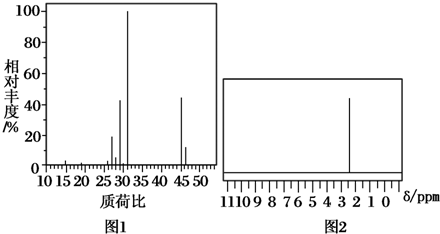
题目内容
2.X、Y、Z是三种短周期元素,在周期表中的相对位置如图所示,有关说法正确的是( )| X | |
| Y | Z |
| A. | X、Y、Z可以都是金属 | |
| B. | 原子半径:Z>Y>X | |
| C. | 最高价氧化物对应的水化物酸性:Z>Y>X | |
| D. | 若X、Y、Z可形成  分子,则其中各原子都满足8电子结构 分子,则其中各原子都满足8电子结构 |
分析 X、Y位于相同主族,Y、Z位于同一周期且相邻,由三种元素的相对位置可知X可为第一周期或第二周期元素,
A.如X为Li,则Y、Z分别为Na、Mg;
B.同周期元素从左到右原子半径逐渐减小;
C.非金属性X>Y,非金属性越强,对应的最高价氧化物对应的水化物酸性越强;
D.若X、Y、Z可形成  分子,应为
分子,应为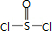 .
.
解答 解:X、Y位于相同主族,Y、Z位于同一周期且相邻,由三种元素的相对位置可知X可为第一周期或第二周期元素,
A.如X为Li,则Y、Z分别为Na、Mg,则都可为金属元素,故A正确;
B.同周期元素从左到右原子半径逐渐减小,则Y>Z,故B错误;
C.非金属性X>Y,非金属性越强,对应的最高价氧化物对应的水化物酸性越强,故C错误;
D.若X、Y、Z可形成  分子,应为
分子,应为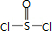 ,S原子不满足8电子结构,故D错误.
,S原子不满足8电子结构,故D错误.
故选A.
点评 本题考查位置、结构、性质的关系及应用,把握元素在周期表中的位置及元素周期律为解答的关键,注意利用实例分析,侧重分析能力和归纳能力的考查,题目难度不大.

练习册系列答案
相关题目
13.某学生在实验室进行化学实验,其中他的操作不正确的是( )
| A. | 取用AgNO3时,应在实验柜中寻找棕色瓶带有滴管的试剂瓶 | |
| B. | 用稀HNO3清洗做过银镜反应后的试管 | |
| C. | 用NaOH溶液清洗沾有硫磺的试管 | |
| D. | 用稀HCl清洗做过高锰酸钾分解实验的试管 |
10.常温下,将NO和O2两种气体按物质的量1:3混合,则其平均相对分子质量是( )
| A. | 40.7 | B. | 46 | C. | 36 | D. | 44 |
17.下列说法正确的是( )
| A. | 3≤原子最外层电子数<8的元素一定是非金属元素 | |
| B. | 原子最外层只有1个电子的元素一定是第ⅠA族元素 | |
| C. | 最外层电子数比次外层电子数多的元素一定是第2周期元素 | |
| D. | 某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第3周期 |
7.有6种物质:①甲烷 ②甲苯 ③聚乙烯 ④丙烯⑤乙醇⑥乙醛,既能使酸性高锰酸钾溶液褪色又能与溴水起反应使之褪色的是( )
| A. | ②③④ | B. | ③④⑥ | C. | ②④⑤ | D. | ④⑥ |
11.对Na、Mg、Al的有关性质的叙述正确的是( )
| A. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | B. | 原子半径:Na<Mg<Al | ||
| C. | 离子的氧化性:Na+>Mg2+>Al3+ | D. | 单质的还原性:Na<Mg<Al |