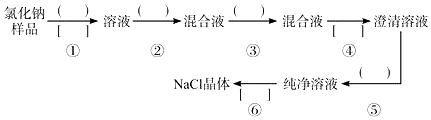
题目内容
1.实验室现有一瓶含少量氯化钙的氯化钾,通过下面的实验制取纯净的氯化钾,根据实验步骤填写下列空白.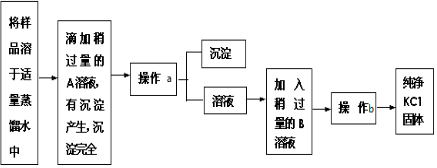
(1)加入的A是K2CO3,检验A是否过量的方法是在上层清夜中继续加入碳酸钾,溶液无沉淀,说明已完全反应.
(2)操作a是过滤,用到的玻璃仪器有烧杯、漏斗、玻璃棒
(3)溶液中加入的B物质是HCl,应加入过量B物质的理由是保证碳酸钾溶液完全反应.
(4)操作b是蒸发,其中用到与操作a相同的玻璃仪器是玻璃棒,该仪器在此处的作用是防止蒸发时液体飞溅.
分析 为除去氯化钾中的氯化钙,将样品溶于水,先加入过量的碳酸钾,即A,生成碳酸钙沉淀,过滤,得到沉淀碳酸钙,滤液中加入稍过量的盐酸,然后进行蒸发结晶,得到氯化钾固体,以此解答该题.
解答 解:(1)由以上分析可知A为K2CO3,为检验碳酸钾是否过量,可在上层清夜中继续加入碳酸钾,溶液无沉淀,说明已完全反应,
故答案为:K2CO3;在上层清夜中继续加入碳酸钾,溶液无沉淀,说明已完全反应;
(2)a为过滤操作,用到的玻璃仪器有烧杯、漏斗、玻璃棒,故答案为:过滤;烧杯;漏斗;玻璃棒;
(3)加入B为盐酸,应过量,以保证碳酸钾溶液完全反应,故答案为:HCl;保证碳酸钾溶液完全反应;
(4)操作b是蒸发,用到与操作a相同的玻璃仪器是玻璃棒,蒸发时,用玻璃棒不断搅拌,以防止蒸发时液体飞溅,故答案为:蒸发;玻璃棒;防止蒸发时液体飞溅.
点评 本题考查物质的分离、提纯,为高频考点,侧重考查学生的分析能力和实验能力,注意把握物质的性质以及实验的操作方法,把握实验的设计,难度不大.

练习册系列答案
相关题目
12.下列有关物质的分类不正确的是( )
| A. | 硫酸(酸) | B. | 溶液(混合物) | C. | Al2O3(两性氧化物) | D. | 纯碱(碱) |
9.下列有关化学用于正确的是( )
| A. | KCl的摩尔质量是:74.5g | B. | 一水合氨的化学式为:NH4•OH | ||
| C. | Na2O2中的阴离子为:O2- | D. | 镁的原子结构示意图如图所示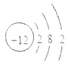 |
16.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 能与铝反应放出氢气的溶液中:K+、Ca2+、Cl-、HCO3- | |
| C. | pH=2的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
10.下列反应中,是吸热反应,也是氧化还原反应的是( )
| A. | Ba(OH)2•8H2O与NH4Cl晶体混合 | B. | 盐酸与NaOH溶液混合 | ||
| C. | 炽热的碳与二氧化碳反应 | D. | Al片投入盐酸中 |
11.下列有关问题,与盐类的水解无关的是( )
| A. | NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 | |
| B. | 盐酸可作铁制品的除锈剂 | |
| C. | 实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 | |
| D. | 将FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 |