题目内容
11.油脂的主要成分是高级脂肪酸的甘油酯,在室温下,植物油脂通常呈液态,叫做油.分析 油脂是高级脂肪酸与甘油形成的酯,油脂是油与脂肪的总称,常温下,油脂中脂肪为固体,油为液体.
解答 解:油脂根据其物质状态可分为油(液态)和脂肪(固态),室温下呈液态的油脂称为油;是不饱和高级脂肪酸与甘油形成的酯,豆油、花生油等植物油在室温下呈液态;室温下呈固态的油脂称为脂,猪油等动物性油在室温下呈固态,油脂在人体内的变化主要是在脂肪酶的催化下,进行水解生成甘油和高级脂肪酸,然后分别进行氧化,释放能量,在人体内提供能量,
故答案为:液;油.
点评 本题考查了油脂的分类,解答本题须正确地认识油和脂的区别与性质,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列各组物质之间通过一步就能实现如图所示转化的是( )
| 物质编号 | 物质转化关系 | a | b | c | d |
| ① | 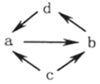 | NO | NO2 | N2 | HNO3 |
| ② | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
| ③ | SiO2 | Na2SiO3 | Si | H2SiO3 | |
| ④ | SO2 | SO3 | S | H2SO4 |
| A. | ①② | B. | ②③ | C. | ②④ | D. | ①③ |
2.下列物质中属于同系物的是( )
①CH3CH2Cl ②CH2=CHCl ③CH3CH2CH2Cl ④CH2ClCH2Cl ⑤CH3CH2CH2CH3⑥CH3CH(CH3)2.
①CH3CH2Cl ②CH2=CHCl ③CH3CH2CH2Cl ④CH2ClCH2Cl ⑤CH3CH2CH2CH3⑥CH3CH(CH3)2.
| A. | ①②④ | B. | ①④ | C. | ①③ | D. | ⑤⑥ |
6.化学在生产和日常生活中有着重要的作用.下列有关说法正确的是( )
| A. | “地沟油”经过加工处理后,可以用来制肥皂 | |
| B. | 二氧化硫有漂白性,大量用作棉,麻、纸张和食品的漂白 | |
| C. | 汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的 | |
| D. | PM2.5颗粒(微粒直径约为2.5×10-6m)分散在空气中形成气溶胶 |
20.CaS可用于制备发光漆、用作脱毛剂、杀虫剂、硫脲等,还用于医药工业、重金属处理及环保中.某化学探究小组在实验室中利用反应:CaSO4+C$\stackrel{高温}{→}$CaS+CaO+SO2↑+CO↑+CO2↑制备硫化钙并检验产物,可选用的装置如下.回答下列问题:
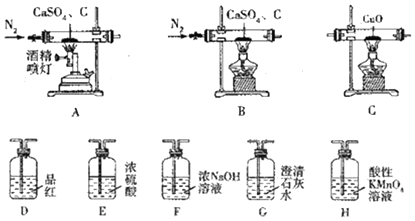
已知:①C及E~H中的试剂均为足量.
②酸性KMnO4溶液作氧化剂时,锰元素被还原成Mn2+
③CaS与H2O反应生成Ca(OH)2和H2S.
(1)实验1:若只检验生成物中是否含有CO,可采用的装置组合为AFECG(AFGECG或AFEC或AC)(按气流方向,填字母组合),生成物中存在CO的现象是装置C中黑色固体变为红色,装置G中澄清石灰水变浑浊.
(2)实验2:若只检验生成物中是否含有CO2,可釆用的最简单的装置组合为AHG(按气流方向,填字母组合),除去SO2的离子方程式为5SO2+2MnO4-+2H2O═2Mn2++5SO42-+4H+.
(3)实验3:若同时检验CO2和SO2,采用的装置组合为ADHG或AHG(按气流方向,填字母组合).
(4)若制备反应的条件完全相同,将产生的气体全部通入上述实验装置中,得到的有关数据如表:
写出CaSO4和焦炭在高温条件下反应生成CaS的化学方程式:2CaSO4+3C$\frac{\underline{\;高温\;}}{\;}$CaS+CaO+SO2↑+2CO2↑+CO↑.
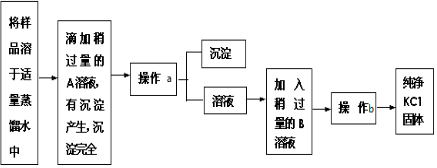
(5)为了证明硫化钙的化学式设计如下实验:将一定质量(m1)的样品溶于足量的饱和Na2CO3溶液中,通过过滤、洗涤、干燥操作,称得固体质量为m2,则表示硫化钙组成的计算式为n(Ca):n(S)=$\frac{{m}_{2}}{100}:\frac{5{m}_{1}-2{m}_{2}}{160}$(用含m1、m2的代数式表示).

已知:①C及E~H中的试剂均为足量.
②酸性KMnO4溶液作氧化剂时,锰元素被还原成Mn2+
③CaS与H2O反应生成Ca(OH)2和H2S.
(1)实验1:若只检验生成物中是否含有CO,可采用的装置组合为AFECG(AFGECG或AFEC或AC)(按气流方向,填字母组合),生成物中存在CO的现象是装置C中黑色固体变为红色,装置G中澄清石灰水变浑浊.
(2)实验2:若只检验生成物中是否含有CO2,可釆用的最简单的装置组合为AHG(按气流方向,填字母组合),除去SO2的离子方程式为5SO2+2MnO4-+2H2O═2Mn2++5SO42-+4H+.
(3)实验3:若同时检验CO2和SO2,采用的装置组合为ADHG或AHG(按气流方向,填字母组合).
(4)若制备反应的条件完全相同,将产生的气体全部通入上述实验装置中,得到的有关数据如表:
| 实验前 | 实验后 | |
| 实验1 | 装置C硬质玻璃管连同CuO质量为26.80g | 装置C硬质玻璃管连同反应后固体质量为26.64g |
| 实验2 | 装置G连同溶液质量为187.50g | 装置G连同反应后溶液及沉淀的质量为188.38g |
| 实验3 | 装置D、H连同溶液质量和为373.60g | 装置D、H连同溶液质量和为374.24g |
(5)为了证明硫化钙的化学式设计如下实验:将一定质量(m1)的样品溶于足量的饱和Na2CO3溶液中,通过过滤、洗涤、干燥操作,称得固体质量为m2,则表示硫化钙组成的计算式为n(Ca):n(S)=$\frac{{m}_{2}}{100}:\frac{5{m}_{1}-2{m}_{2}}{160}$(用含m1、m2的代数式表示).
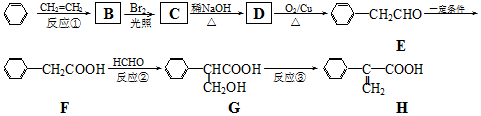
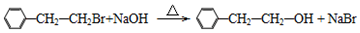 .
.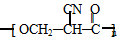 (要重新写过) 的合成路线:NCCH2CHO$→_{△}^{新制Cu(OH)_{2}}$ $\stackrel{H+}{→}$
(要重新写过) 的合成路线:NCCH2CHO$→_{△}^{新制Cu(OH)_{2}}$ $\stackrel{H+}{→}$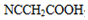 →
→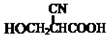 →
→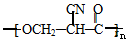 .
.