题目内容
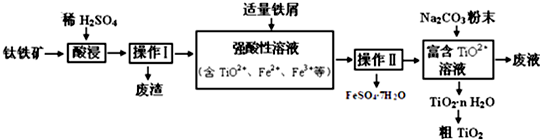
18.垃圾是放错地方的资源,工业废料也可以再利用.某化学兴趣小组在实验室中用废弃的含铝、铁、铜的合金制取硫酸铝溶液、硝酸铜晶体和铁红(Fe2O3).实验方案如下:
(1)滤渣B中发生反应的离子反应方程式为:NO3-+Fe+4H+=Fe3++NO↑+2H2O;2NO3-+3Cu+8H+=3Cu2++2NO↑+4H2O.
(2)已知Fe(OH)3沉淀的pH是3~4,溶液C通过调节pH可以使Fe3+沉淀完全.下列物质中可用作调整溶液C的pH的试剂是CD(填序号).
A.铜粉B.氨水C.氢氧化铜D.碱式碳酸铜
(3)常温,若溶液C中金属离子均为1mol•L-1,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cu(OH)2]=2.2×10-20.控制pH=4,溶液中c(Fe3+)=4x10-8mol•L-1.
(4)将20mL Al2(SO4)3溶液与等物质的量浓度的Ba(OH)2溶液70mL混合,反应的离子方程为2Al3++3SO42-+3Ba2++7OH-=3BaSO4↓+Al(OH)3↓+AlO2-+2H2O.
(5)在0.1L的混合酸溶液中,c(HNO3)=2mol•L-1,c(H2SO4)=3mol•L-1,将0.3mol的铜放入加热充分反应后,所得溶液的溶质的物质的量浓度为0.3mol/L.(溶液体积不变)
分析 含铝、铁、铜的合金与足量KOH作用,反应后所得滤液A为KAlO2,滤渣B为铁和铜,B中加入硝酸,得到的溶液C为硝酸铜和硝酸铁的混合物,铁离子易水解,可通过调节溶液pH的方法得到氢氧化铁沉淀,即E为氢氧化铁,D为硝酸铜溶液,经蒸发、结晶可得到硝酸铜晶体,
(1)滤渣B为铁和铜,B中加入硝酸,得到的溶液C为硝酸铜和硝酸铁的混合物;
(2)溶液C通过调节pH可以使Fe3+沉淀完全,加入的物质能消耗氢离子,但是不能引入新的杂质;
(3)根据Ksp[Fe(OH)3]和溶液中氢氧根离子的浓度计算c(Fe3+);
(4)将20mL Al2(SO4)3溶液与等物质的量浓度的Ba(OH)2溶液70mL混合,则二者的物质的量之比为2:7,根据物质的量关系写方程式;
(5)根据反应3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O进行判断.
解答 解:含铝、铁、铜的合金与足量KOH作用,反应后所得滤液A为KAlO2,滤渣B为铁和铜,B中加入硝酸,得到的溶液C为硝酸铜和硝酸铁的混合物,铁离子易水解,可通过调节溶液pH的方法得到氢氧化铁沉淀,即E为氢氧化铁,D为硝酸铜溶液,经蒸发、结晶可得到硝酸铜晶体,
(1)滤渣B为铁和铜,B中加入硝酸,得到的溶液C为硝酸铜和硝酸铁的混合物,反应的离子方程式为NO3-+Fe+4H+=Fe3++NO↑+2H2O,2NO3-+3Cu+8H+=3Cu2++2NO↑+4H2O;
故答案为:NO3-+Fe+4H+=Fe3++NO↑+2H2O;2NO3-+3Cu+8H+=3Cu2++2NO↑+4H2O;
(2)溶液C通过调节pH可以使Fe3+沉淀完全,应加入CuO、碱式碳酸铜或氢氧化铜,而加入铜粉生成Fe2+,加入氨水引入新的杂质,
故答案为:CD;
(3)已知溶液的pH=4,则c(H+)=10-4mol/L,c(OH-)=10-10mol/L,Ksp[Fe(OH)3]=4.0×10-38=c(Fe3+)×c3(OH-),所以c(Fe3+)=4.0×10-8mol/L;
故答案:4.0×10-8;
(4)将20mL Al2(SO4)3溶液与等物质的量浓度的Ba(OH)2溶液70mL混合,则二者的物质的量之比为2:7,则反应时铝离子与氢氧根离子的物质的量之比为1:3.5,所以有部分氢氧化铝转化为偏铝酸根离子,其离子方程式为:2Al3++3SO42-+3Ba2++7OH-=3BaSO4↓+Al(OH)3↓+AlO2-+2H2O;
故答案为:2Al3++3SO42-+3Ba2++7OH-=3BaSO4↓+Al(OH)3↓+AlO2-+2H2O;
(5)n(HNO3)=0.1L×2mol/L=0.2mol,n(H2SO4)=0.1L×3mol/L=0.3mol,
则n(H+)=0.2mol+2×0.3mol=0.8mol,n(NO3-)=0.2mol,n(Cu)=0.3mol,
由反应3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知,0.3mol完全反应生成0.3mol硫酸铜,则c(CuSO4)=$\frac{0.3mol}{0.1L}$=0.3mol/L;
故答案为:0.3mol/L.
点评 本题主要考查了物质的分离提纯和制备,题目涉及离子反应方程式的书写、除杂质、氧化还原反应、溶度积的有关计算等,综合性较强,题目难度中等,侧重于考查学生对基础知识的综合应用能力.

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案 学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:(A)移取25.00mL待测的盐酸溶液,加入1-2滴酚酞试剂
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)BDCEAF,本实验中的标准溶液装在图中的乙中,若某实验中需要用高锰酸钾进行滴定,则选择图中的甲.
(2)上述(B)操作的目的是防止将标准液稀释.
(3)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)偏大.
(4)实验中用左手控制碱式滴定管橡皮管玻璃珠处(填仪器及部位),眼睛注视锥形瓶中溶液的颜色变化,直至滴定终点.判断到达终点的现象是锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色.
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对测定结果的影响是偏小.
(6)滴定结束后如仰视观察滴定管中液面刻度,则对滴定结果的影响是偏大
(7)滴定结果
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
| A. | 温度过高对合成氨不利 | |
| B. | 合成氨在高压下进行是有利的 | |
| C. | 高温及加入催化剂都能使合成氨的反应速率加快 | |
| D. | 增加N2的浓度可提高平衡混合物中NH3的含量 |
| A. | 向被污染的土壤洒石灰 | |
| B. | 向远离污染源的高处撤离 | |
| C. | 用浸有纯碱溶液的毛巾捂住口鼻迅速撤离 | |
| D. | 来不及撤离时可用纯碱溶液浸湿的棉被堵好门窗 |