题目内容
8.某工厂发生CI2泄漏,以下应对措施中主要是基于CI2的物理性质考虑的是( )| A. | 向被污染的土壤洒石灰 | |
| B. | 向远离污染源的高处撤离 | |
| C. | 用浸有纯碱溶液的毛巾捂住口鼻迅速撤离 | |
| D. | 来不及撤离时可用纯碱溶液浸湿的棉被堵好门窗 |
分析 A.石灰溶于水形成氢氧化钙是碱溶液可以吸收氯气;
B.氯气密度比空气重;
C.纯碱是碳酸钠溶液可以和氯气发生反应吸收氯气;
D.纯碱是碳酸钠溶液可以和氯气发生反应吸收氯气;
解答 解:A.石灰溶于水形成氢氧化钙是碱溶液可以吸收氯气,利用的是氯气的化学性质,故A错误;
B.氯气密度比空气重,发生CI2泄漏向远离污染源的高处撤离,故B正确;
C.纯碱是碳酸钠溶液可以和氯气发生反应吸收氯气,氯气密度比空气重用浸有纯碱溶液的毛巾捂住口鼻迅速撤离,故C错误;
D.纯碱是碳酸钠溶液可以和氯气发生反应吸收氯气,来不及撤离时可用纯碱溶液浸湿的棉被堵好门窗,故D错误;
故选B.
点评 本题考查了氯气的物理性质、化学性质及其性质的应用,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
19.现有部分短周期元素的性质或原子结构如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是614C;
(2)实验室检验Y元素的气态氢化物的方法和现象是用湿润的红色石蕊试纸检验,试纸变蓝;
(3)Z元素与氢元素、氧元素形成的化合物HZO有漂白性,其结构式为H-O-Cl;
(4)探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是H2CO3(填分子式),理由是H2CO3是弱酸,其余均为强酸;
(5)将T元素的氧化物TO2和Z的单质同时通入水中,可发生反应,该反应化学方程式为Cl2+SO2+2H2O=2HCl+H2SO4.
| 元素编号 | 元素性质或原子结构 |
| T | 最外层电子占核外电子总数的$\frac{3}{8}$ |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)实验室检验Y元素的气态氢化物的方法和现象是用湿润的红色石蕊试纸检验,试纸变蓝;
(3)Z元素与氢元素、氧元素形成的化合物HZO有漂白性,其结构式为H-O-Cl;
(4)探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是H2CO3(填分子式),理由是H2CO3是弱酸,其余均为强酸;
(5)将T元素的氧化物TO2和Z的单质同时通入水中,可发生反应,该反应化学方程式为Cl2+SO2+2H2O=2HCl+H2SO4.
13.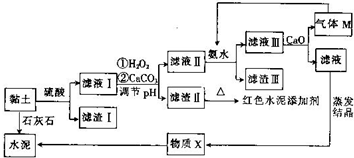 土壤是人类赖以生存的最基本物质,以黏土为原料生产的产品伴随着人类文明的脚步.皖北名胜皇藏峪的黏土,水浸不塌,是生产无机非金属材料的优质原料.某兴趣小组以当地黏土为原料探究彩色水泥、轻质耐火材料的联合生产,其设计的流程如图所示.
土壤是人类赖以生存的最基本物质,以黏土为原料生产的产品伴随着人类文明的脚步.皖北名胜皇藏峪的黏土,水浸不塌,是生产无机非金属材料的优质原料.某兴趣小组以当地黏土为原料探究彩色水泥、轻质耐火材料的联合生产,其设计的流程如图所示.
已知:黏土的主要成分为2CaO•3Al2O3•FeO•Fe2O3•10SiO2•nH2O.部分难溶物开始沉淀时和完全沉淀时的pH如表所示.
(1)为提高酸浸速率,除适当增大硫酸浓度外,还可采取的措施有搅拌、适当升温或将研磨黏土(任写一条).
(2)向滤液Ⅰ中加入H2O2的作用是将滤液中的Fe2+氧化为Fe3+;用CaCO3调节溶液pH约为3.3,其目的是使Fe3+完全转化为Fe(OH)3沉淀而除去.
(3)红色水泥添加剂的主要成分是Fe2O3.
(4)物质X的化学式为CaSO4•2H2O.
(5)气体M的电子式为 ;向滤液Ⅲ中加放CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).
;向滤液Ⅲ中加放CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).
(6)氮化铝广泛用于电子陶瓷等工业领域,以滤渣Ⅲ、碳及氮气为原料可制备氮化铝,用化学方程式表示制备过程:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O、Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO.
 土壤是人类赖以生存的最基本物质,以黏土为原料生产的产品伴随着人类文明的脚步.皖北名胜皇藏峪的黏土,水浸不塌,是生产无机非金属材料的优质原料.某兴趣小组以当地黏土为原料探究彩色水泥、轻质耐火材料的联合生产,其设计的流程如图所示.
土壤是人类赖以生存的最基本物质,以黏土为原料生产的产品伴随着人类文明的脚步.皖北名胜皇藏峪的黏土,水浸不塌,是生产无机非金属材料的优质原料.某兴趣小组以当地黏土为原料探究彩色水泥、轻质耐火材料的联合生产,其设计的流程如图所示.已知:黏土的主要成分为2CaO•3Al2O3•FeO•Fe2O3•10SiO2•nH2O.部分难溶物开始沉淀时和完全沉淀时的pH如表所示.
| Fe(OH)2 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀时的pH | 6.3 | 1.9 | 3.4 |
| 完全沉淀时的pH | 8.3 | 3.2 | 4.7 |
(2)向滤液Ⅰ中加入H2O2的作用是将滤液中的Fe2+氧化为Fe3+;用CaCO3调节溶液pH约为3.3,其目的是使Fe3+完全转化为Fe(OH)3沉淀而除去.
(3)红色水泥添加剂的主要成分是Fe2O3.
(4)物质X的化学式为CaSO4•2H2O.
(5)气体M的电子式为
 ;向滤液Ⅲ中加放CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).
;向滤液Ⅲ中加放CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).(6)氮化铝广泛用于电子陶瓷等工业领域,以滤渣Ⅲ、碳及氮气为原料可制备氮化铝,用化学方程式表示制备过程:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O、Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO.
20.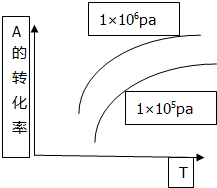 反应mA(g)+B(s)?pC(g)+qD(g)△H>0中A的转化率和温度(T)、压强(P)的关系如图曲线,下列结论正确的是( )
反应mA(g)+B(s)?pC(g)+qD(g)△H>0中A的转化率和温度(T)、压强(P)的关系如图曲线,下列结论正确的是( )
 反应mA(g)+B(s)?pC(g)+qD(g)△H>0中A的转化率和温度(T)、压强(P)的关系如图曲线,下列结论正确的是( )
反应mA(g)+B(s)?pC(g)+qD(g)△H>0中A的转化率和温度(T)、压强(P)的关系如图曲线,下列结论正确的是( )| A. | 逆反应为放热反应m<p+q | B. | 逆反应为吸热反应m>p+q | ||
| C. | 正反应为放热反应m<p+q | D. | 正反应为吸热反应m>p+q |
17.某有机物在氧气中充分燃烧,生成的二氧化碳和水的物质的量之比为1:1,由此可得出的正确结论是( )
| A. | 该有机物分子中碳、氢、氧原子个数比为1:2:3 | |
| B. | 该有机物分子中碳、氢原子个数比为1:2 | |
| C. | 该有机物中肯定含氧 | |
| D. | 可以判断该有机物中是否含氧 |
18.下列物质中属于电解质的是( )
| A. | H2 | B. | Na2SO4 | C. | C2H5OH | D. | CO2 |
