题目内容
9.常温下,用0.10mol/LNaOH溶液滴定20.00mL稀醋酸(HAc),下列说法中正确的是( )| A. | 当混合溶液的pH>7时,其中不可能存在HAc分子 | |
| B. | 当混合溶液的pH<7时,混合液中c(Na+)>c((Ac-) | |
| C. | 判断该滴定过程的终点,最好选择甲基橙作为指示剂 | |
| D. | 达到滴定终点时,混合液中c(Na+)和c((Ac-)一定不相等 |
分析 A.醋酸为弱酸,醋酸根离子存在水解评价,则混合液中一定存在醋酸分子;
B.pH<7的溶液呈酸性,则c(H+)>c((OH-),结合电荷守恒判断;
C.恰好反应时生成醋酸钠,溶液呈碱性,而甲基橙的变色范围为3.1-4.4,以甲基橙作为指示剂,滴定终点与反应终点差距大,导致误差较大;
D.达到滴定终点时溶质为醋酸钠,醋酸根离子发生水解,则c(Na+)>c((Ac-).
解答 解:A.由于醋酸根离子的水解反应为可逆反应,则反应后溶液中一定存在HAc分子,故A错误;
B.当混合溶液的pH<7时,溶液呈酸性,则c(H+)>c((OH-),结合电荷守恒可知:c(Na+)>c((Ac-),故B错误;
C.用0.10mol/LNaOH溶液滴定20.00mL稀醋酸(HAc),恰好反应时生成醋酸钠,醋酸根离子水解溶液呈碱性,由于甲基橙的变色范围为3.1-4.4,以酚酞作为指示剂滴定至终点更准确,故C错误;
D.达到滴定终点时,反应后溶质为醋酸钠,由于醋酸根离子发生水解,则混合液中c(Na+)和c((Ac-)一定不相等,故D正确;
故选D.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确电荷守恒、盐的水解原理为解答关键,注意掌握溶液酸碱性与溶液pH的关系,C为易错点,注意指示剂的变色范围,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
20.某实验中得到A、B、C三种液体的混合物,其信息如表:
欲分离上述混合物获得C,下列说法正确的是( )
| 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解性 | |
| A | 78 | 0.8786 | 80 | A,B,C互溶 |
| B | 74 | 0.81018 | 108 | |
| C | 130 | 0.8670 | 142 |
| A. | 不能用蒸馏的方法进行分离 | |
| B. | 可以用过滤的方法进行分离 | |
| C. | 若采用蒸馏操作,冷凝管中冷却水的流向应该与蒸气的流向相反 | |
| D. | 该实验中用到的玻璃仪器有:酒精灯、蒸溜烧瓶、冷凝管、接液管、锥形瓶 |
17.电视连续剧《大宋提刑官》中的主人公宋慈在案件侦破中常使用“银针验毒”,“银针验毒”的原理是 4Ag+2H2S+O2═2X+2H2O,下列有关说法中正确的是( )
| A. | X 的化学式为AgS | |
| B. | 每生成1molX会转移2 mol电子 | |
| C. | 反应中Ag、H2S均是还原剂 | |
| D. | 银针验毒时,空气中的氧气发生氧化反应 |
4.下列属于弱电解质的是( )
| A. | CO2 | B. | BaSO4 | C. | HClO | D. | Cl2 |
14.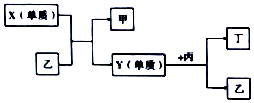 现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )
现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )
 现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )
现有W、X、Y、Z四种短周期元素,W分别与X、Y、Z结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子的分子.Y、Z结合生成化合物丁.有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图,下列说法正确的是( )| A. | 原子半径的大小:W<Y<Z<X | B. | 单质与H2化合的难易程度:X>Y | ||
| C. | 甲与丙反应不可能生成离子化合物 | D. | Z的最高价氧化物的水化物为强酸 |
1.“笑气”(N2O)是最早应用于医疗的麻醉剂之一.有关理论认为N2O与CO2分子具有相似的结构(包括电子式),且氧原子只与一个氮原子相连.下列说法合理的( )
| A. | N2O与CO2化学性质完全相同 | B. | N2O的电子式可表示: | ||
| C. | N2O与CO2均不含非极性键 | D. | N2O为三角形分子 |
18.化学科学对提高人类生活质量和促进社会发展具有重要作用,下列说法正确的是( )
| A. | CsICl2常用于化学上的分子筛技术,它既有氧化性又有还原性,CsICl2有还原性是因为有较强还原性的I- | |
| B. | “神舟十一号”宇宙飞船成功与“天宫二号”对接,其太阳能光电池材料是硅 | |
| C. | 司母戊鼎、辽宁舰甲板、超轻钨碳塑钢眼镜框架等原材料属合金 | |
| D. | 硅橡胶能耐高温和耐低温是新型的无机非金属材料 |