题目内容
氧氮杂?是新药研制过程中发现的一类重要活性物质,能用于改善大脑缺血.下面是某研究小组提出的一种氧氮杂?类化合物E的合成路线:
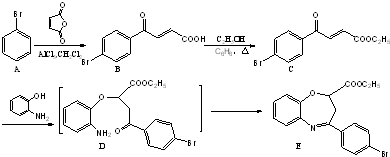
(1)化合物B 中的含氧官能团为 和 (填官能团名称).
(2)D→E经历两步反应,其反应类型依次为 和 .
(3)写出同时满足下列条件的C的一种同分异构体的结构简式: .
Ⅰ.分子中含有1个苯环;
Ⅱ.能发生银镜反应;
Ⅲ.分子中有3种不同化学环境的氢.
(4)D合成E时还可能生成副产物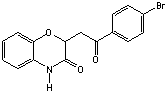 和一种常见的有机物F,F的结构简式为 .
和一种常见的有机物F,F的结构简式为 .
(5)已知: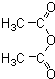
CH3COOH.原料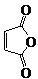 俗名“马莱酐”,它是马莱酸(顺丁烯二酸:)的酸酐.
俗名“马莱酐”,它是马莱酸(顺丁烯二酸:)的酸酐.
请写出以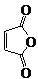 为原料制备化合物
为原料制备化合物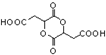 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
CH3CH2OH
CH2=CH2
Br-CH2CH2-Br.

(1)化合物B 中的含氧官能团为
(2)D→E经历两步反应,其反应类型依次为
(3)写出同时满足下列条件的C的一种同分异构体的结构简式:
Ⅰ.分子中含有1个苯环;
Ⅱ.能发生银镜反应;
Ⅲ.分子中有3种不同化学环境的氢.
(4)D合成E时还可能生成副产物
 和一种常见的有机物F,F的结构简式为
和一种常见的有机物F,F的结构简式为(5)已知:
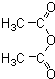
| H2O |
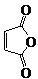 俗名“马莱酐”,它是马莱酸(顺丁烯二酸:)的酸酐.
俗名“马莱酐”,它是马莱酸(顺丁烯二酸:)的酸酐.请写出以
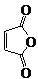 为原料制备化合物
为原料制备化合物 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CH2OH
| 浓H2SO4 |
| 170℃ |
| Br2 |
考点:有机物的合成
专题:有机物的化学性质及推断
分析:(1)根据B的结构简式可判断;
(2)D→E经历两步反应,氨基与羰基先加成,再脱去一分子水,据此答题;
(3)C的一种同分异构体满足Ⅰ.分子中含有1个苯环;Ⅱ.能发生银镜反应,说明有醛基;Ⅲ.分子中有3种不同化学环境的氢,以此分析结构简式;
(4)比较D和E的结构简式以及副产物 ,利用元素守恒可推断另一物质F;
,利用元素守恒可推断另一物质F;
(5)先以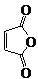 为原料制备化合物
为原料制备化合物 ,要先将
,要先将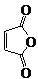 水解得
水解得 ,再与溴化氢加成,再水解、酸化、酯化可得产品.
,再与溴化氢加成,再水解、酸化、酯化可得产品.
(2)D→E经历两步反应,氨基与羰基先加成,再脱去一分子水,据此答题;
(3)C的一种同分异构体满足Ⅰ.分子中含有1个苯环;Ⅱ.能发生银镜反应,说明有醛基;Ⅲ.分子中有3种不同化学环境的氢,以此分析结构简式;
(4)比较D和E的结构简式以及副产物
 ,利用元素守恒可推断另一物质F;
,利用元素守恒可推断另一物质F;(5)先以
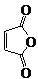 为原料制备化合物
为原料制备化合物 ,要先将
,要先将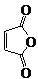 水解得
水解得 ,再与溴化氢加成,再水解、酸化、酯化可得产品.
,再与溴化氢加成,再水解、酸化、酯化可得产品.解答:
解:(1)根据B的结构简式可判断B 中的含氧官能团为羧基和羰基,故答案为:羧基;羰基;
(2)D→E经历两步反应,氨基与羰基先加成,再脱去一分子水,所以其反应类型依次为加成反应、消去反应,故答案为:加成反应;消去反应;
(3)C的一种同分异构体满足Ⅰ.分子中含有1个苯环;Ⅱ.能发生银镜反应,说明有醛基;Ⅲ.分子中有3种不同化学环境的氢,符合上述条件的结构简式为 ,故答案为:
,故答案为: ;
;
(4)比较D和E的结构简式以及副产物 ,利用元素守恒可推断另一物质F为乙醇,结构简式为CH3CH2OH,
,利用元素守恒可推断另一物质F为乙醇,结构简式为CH3CH2OH,
故答案为:CH3CH2OH;
(5)先以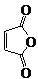 为原料制备化合物
为原料制备化合物 ,要先将
,要先将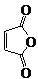 水解得
水解得 ,再与溴化氢加成,再水解、酸化、酯化可得产品,具体合成路线为
,再与溴化氢加成,再水解、酸化、酯化可得产品,具体合成路线为 ,
,
故答案为: .
.
(2)D→E经历两步反应,氨基与羰基先加成,再脱去一分子水,所以其反应类型依次为加成反应、消去反应,故答案为:加成反应;消去反应;
(3)C的一种同分异构体满足Ⅰ.分子中含有1个苯环;Ⅱ.能发生银镜反应,说明有醛基;Ⅲ.分子中有3种不同化学环境的氢,符合上述条件的结构简式为
 ,故答案为:
,故答案为: ;
;(4)比较D和E的结构简式以及副产物
 ,利用元素守恒可推断另一物质F为乙醇,结构简式为CH3CH2OH,
,利用元素守恒可推断另一物质F为乙醇,结构简式为CH3CH2OH,故答案为:CH3CH2OH;
(5)先以
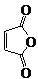 为原料制备化合物
为原料制备化合物 ,要先将
,要先将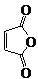 水解得
水解得 ,再与溴化氢加成,再水解、酸化、酯化可得产品,具体合成路线为
,再与溴化氢加成,再水解、酸化、酯化可得产品,具体合成路线为 ,
,故答案为:
 .
.
点评:本题主要考查了有机推断与合成,中等难度,答题时注意要充分利用题目中的信息与基础知识有机结合起来,有机合成路线的设计是本题的难点.

练习册系列答案
相关题目
下列电子式中,书写正确的是( )
A、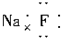 |
B、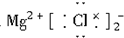 |
C、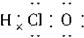 |
D、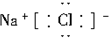 |
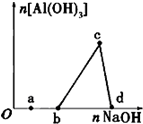 一定量的酸性AlCl3 溶液中逐滴加入NaOH溶液,生成沉淀Al(OH)3的量随NaOH加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
一定量的酸性AlCl3 溶液中逐滴加入NaOH溶液,生成沉淀Al(OH)3的量随NaOH加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A、a点对应的溶液中:K+、Ag+、Ca2+、NO3- |
| B、b点对应的溶液中:K+、NH4+、CO32-、SO42- |
| C、c点对应的溶液中:Na+、Fe3+、SO42-、HCO3- |
| D、d点对应的溶液中:Na+、S2-、SO42-、Cl- |
下列各组离子在指定条件下,一定能大量共存的是( )
| A、pH=1的无色溶液:Na+、Cu2+、NO3-、SO42- |
| B、能溶解Al(OH)3固体的溶液:K+、Na+、HCO3-、NO3- |
| C、能使碘化钾淀粉试纸变蓝的溶液:K+、Fe2+、SO42-、Cl- |
| D、水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、Cl-、NO3- |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1mol过氧化钠与水反应转移电子数为NA |
| B、0.1mol氯化铁水解制成胶体,所得胶体粒子数为0.1NA |
| C、标准状况下,22.4L水中含有水分子数为NA |
| D、1L 0.1mol每升乙酸溶液中氢离子数为0.1NA |
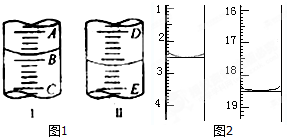

 )和CH2=CH2为原料制备有机物
)和CH2=CH2为原料制备有机物 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).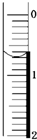 化工试剂草酸钠常用于制革、烟火、整理织物等.纯Na2C2O4为白色晶体,溶于水,不溶于乙醇,有还原性.实验室可用标准KMnO4溶液测定市售草酸钠中Na2C2O4的质量分数(假设杂质不与KMnO4反应).
化工试剂草酸钠常用于制革、烟火、整理织物等.纯Na2C2O4为白色晶体,溶于水,不溶于乙醇,有还原性.实验室可用标准KMnO4溶液测定市售草酸钠中Na2C2O4的质量分数(假设杂质不与KMnO4反应).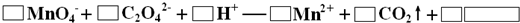
 为测定碳酸钙纯度(设含杂质SiO2),学生设计了如下几个实验方案.请回答每个方案中提出的问题.
为测定碳酸钙纯度(设含杂质SiO2),学生设计了如下几个实验方案.请回答每个方案中提出的问题.