题目内容
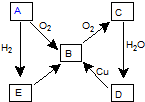 图表示某气态单质A及其化合物之间的转化关系 (某些产物和反应条件已略去).
图表示某气态单质A及其化合物之间的转化关系 (某些产物和反应条件已略去).(1)A单质的电子式
(2)写出E生成B的化学方程式:
(3)①写出由D生成B的离子方程式
②常温下D和E恰好完全反应后溶液的pH
考点:无机物的推断,含氮物质的综合应用
专题:氮族元素
分析:转化图表示某气态单质A及其化合物之间的转化关系,气体A和氧气反应生成B,B和氧气反应生成C,C溶于水生成D,D和铜常温反应生成B,说明D为硝酸,C为NO2,B为NO,E为NH3,A为N2;结合推断分析回答问题;
解答:
解:转化图表示某气态单质A及其化合物之间的转化关系,气体A和氧气反应生成B,B和氧气反应生成C,C溶于水生成D,D和铜常温反应生成B,说明D为硝酸,C为NO2,B为NO,E为NH3
(1)A单质为氮气,氮原子间形成三个共价键,氮气的电子式为: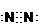 ;
;
故答案为: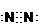 ;
;
(2)E生成B的反应是氨气的催化氧化反应,反应的化学方程式为:4NH3+5O2
4NO+6H2O;
故答案为:4NH3+5O2
4NO+6H2O;
(3)①D生成B的反应是硝酸和铜反应生成硝酸铜,一氧化氮和水,反应的离子方程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
②常温下D和E恰好完全反应生成硝酸铵,溶液中铵根离子水解溶液呈酸性,溶液的pH<7;
故答案为:pH小于7,理由是硝酸铵是强酸弱碱盐,铵根离子水解呈酸性;
(1)A单质为氮气,氮原子间形成三个共价键,氮气的电子式为:
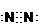 ;
;故答案为:
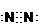 ;
;(2)E生成B的反应是氨气的催化氧化反应,反应的化学方程式为:4NH3+5O2
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(3)①D生成B的反应是硝酸和铜反应生成硝酸铜,一氧化氮和水,反应的离子方程式为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
②常温下D和E恰好完全反应生成硝酸铵,溶液中铵根离子水解溶液呈酸性,溶液的pH<7;
故答案为:pH小于7,理由是硝酸铵是强酸弱碱盐,铵根离子水解呈酸性;
点评:本题考查了物质性质的分析判断,反应特征和条件的熟练掌握,物质性质和反应产物判断是关键,题目较简单.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、在干冰晶体中,与一个CO2分子相邻且等距离的CO2分子共有12个 |
| B、在SiO2晶体中,若含有1molSi原子,则Si-O键数为4NA |
| C、在金刚石晶体中,一个碳原子被12个六元碳环所共用,一个C-C键最多可形成6个六元环,一个六元环实际拥有一个碳原子 |
| D、mg石墨中,正六边形数目为m NA/24,每个环拥有碳原子数与C-C键数之比为2:3 |
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2下列有关该电池的说法不正确的是( )
| A、电池的电解质溶液为碱性溶液,正极为Ni2O3、负极为Fe |
| B、电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| C、电池放电过程中,溶液中的OH-向负极移动 |
| D、电池放电与充电过程发生的化学反应是可逆反应 |
使反应4NH3(g)+3O2(g)=2N2(g)+6H2O(g)在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol.此反应的平均速率v(X)为( )
| A、v (NH3)=0.05mol?L-1?s-1 |
| B、v(O2)=0.015mol?L-1.s-1 |
| C、v(N2)=0.02mol?L-1?s-1 |
| D、v(H2O)=0.02mol?L-1?S-1 |
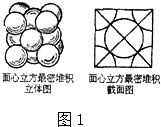 (1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是
(1)现有以下几种物质::①晶体二氧化硅②干冰③五氯化磷④金刚石⑤过氧化钠⑥冰⑦碳化硅⑧白磷;请用编号填写:通过非极性键形成原子晶体的是